含硫芳香化合物广泛存在于药物、农业化学品、有机导电材料和高分子中(图1a)。另外,芳香硫醚可以作为制备相应的亚砜,砜以及苯并噻吩的反应中间体。当前制备芳香硫醚化合物的方法主要依赖于芳香卤代烃和硫醇的亲核芳香取代反应或者交叉偶联反应,这两种方法都在芳香卤代烃的原位形成碳−硫键,因此新引入硫代基团的位置局限于底物中原先卤素的位置。另一方面,通过碳−氢键硫化反应在底物没有预先官能团化的位置引入硫代基团具有很大的吸引力。然而,这种方法通常需要预先引入导向基或者采用富电子的芳香烃从而实现对位点选择性的控制。
钯/降冰片烯催化(Catellani反应)在制备多取代芳香化合物方面具有非常广泛的应用。与传统的芳环官能团化反应相比,这种反应可以对简单芳香卤代烃的邻位和原位同时进行双官能团化(图1b)。该反应具有非常好的位置选择性,在反应中形成的芳基-降冰片烯-钯中间体(ANP)可以与亲电试剂(邻位)和亲核试剂(原位)反应从而实现位置选择性的双官能团化。尽管亲核试剂的选择范围非常广泛,亲电试剂的选取目前还存在着很大的限制,因为亲电试剂必须在有零价钯存在的条件下选择性地与ANP反应,并且亲电试剂与亲核试剂以及降冰片烯必须完全兼容。目前可选的亲电试剂主要限制在碳亲电试剂和氮亲电试剂。因此,通过钯/降冰片烯协同催化在芳环邻位引入别的杂原子具有很大的挑战。
芝加哥大学化学学院董广彬教授(点击查看介绍)课题组成功发展了一种钯/降冰片烯协同催化碘苯的邻位硫化反应(图1c)。作者通过设计一种新型大位阻的硫酰胺亲电试剂成功在碘苯邻位引入包括芳基硫和烷基硫在内的多种硫代基团,并且芳基原位可以发生Heck、Suzuki以及Sonogashira偶联反应。
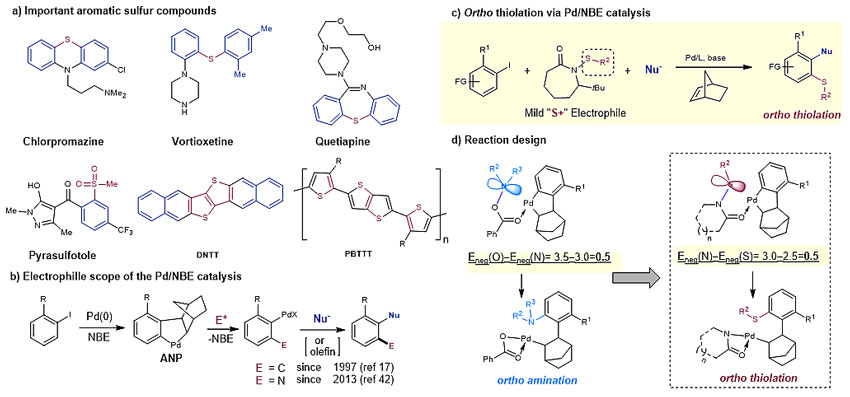
图1 反应背景
作者认为设计一种稳定但是同时具有一定反应活性的硫亲电试剂非常重要。基于之前发展的碘苯邻位胺基化反应的经验,作者选取的硫酰胺作为亲电试剂。这是因为: 1)氮和氧的电负性差距与硫和氮的电负性差距相匹配 (图1d)。2)酰胺的羰基可以作为导向基团从而促进亲电试剂与ANP中间体的反应。值得一提的是Zhenhua Gu课题组几乎在同一时间报道了类似的芳环邻位硫化反应,但是采用了硫代磺酸盐作为亲电试剂。
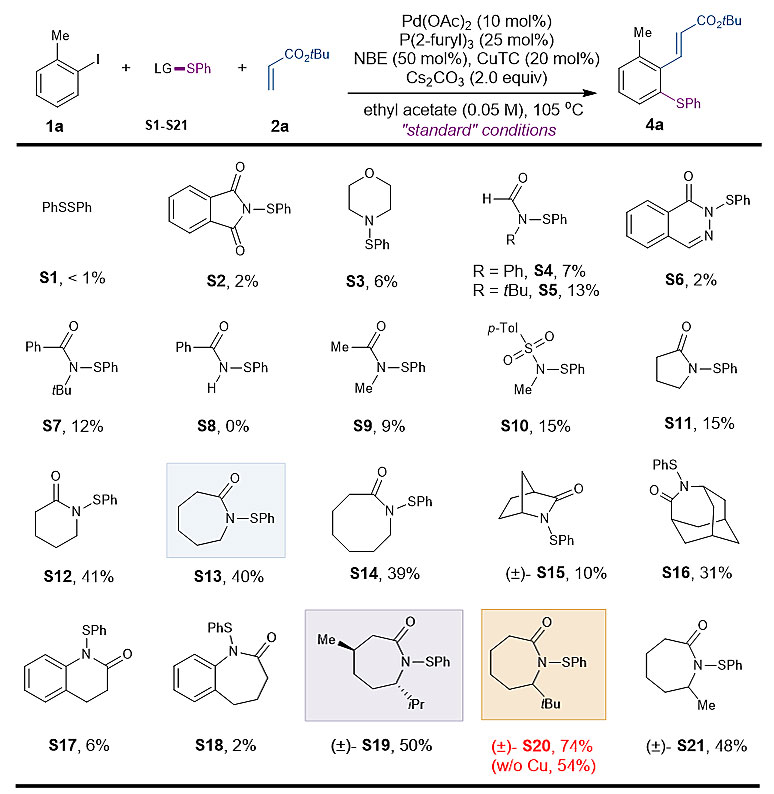
图2 硫酰胺试剂的筛选
作者通过对一系列硫酰胺试剂筛选最终发现叔丁基取代的亲电试剂S20可以得到最高的反应产率(图2)。为了更好地理解这一独特的现象作者对其中六个硫酰胺试剂进行了x射线单晶衍射表征并且得到了其晶体结构。作者发现酰胺旁边的大位阻基团(叔丁基)可以显著增加氮−硫键长,从而削弱了氮−硫键并增加了亲电试剂的反应活性(图3)。
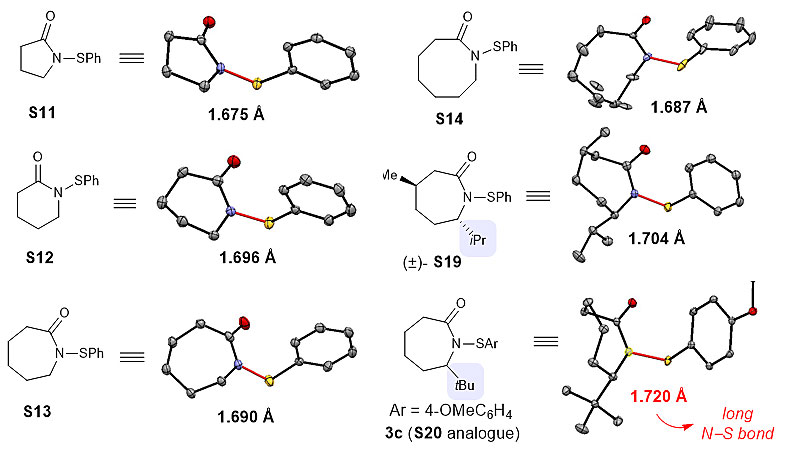
图3 硫酰胺试剂的晶体结构
该反应具有非常好的底物普适性和官能团兼容性(图4-5)。含有卤素、酯基、Weinreb酰胺、胺基等官能团在内的36种底物都可以在标准条件下得到相对应的邻位硫化产物。值得一提的是,一系列稠环和杂环底物也表现出不错的反应性。除了芳基硫,烷基硫同样可以被引入到碘苯的邻位(5k)。
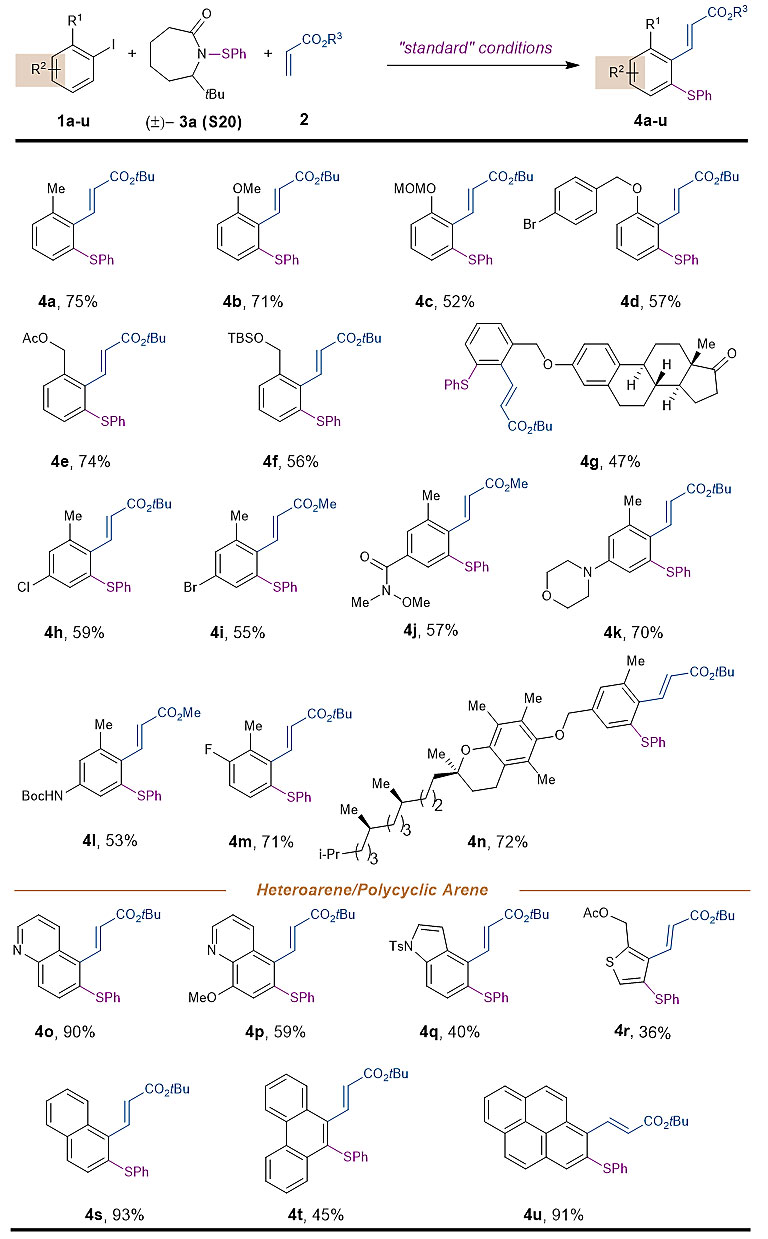
图4 芳基碘代物底物拓展
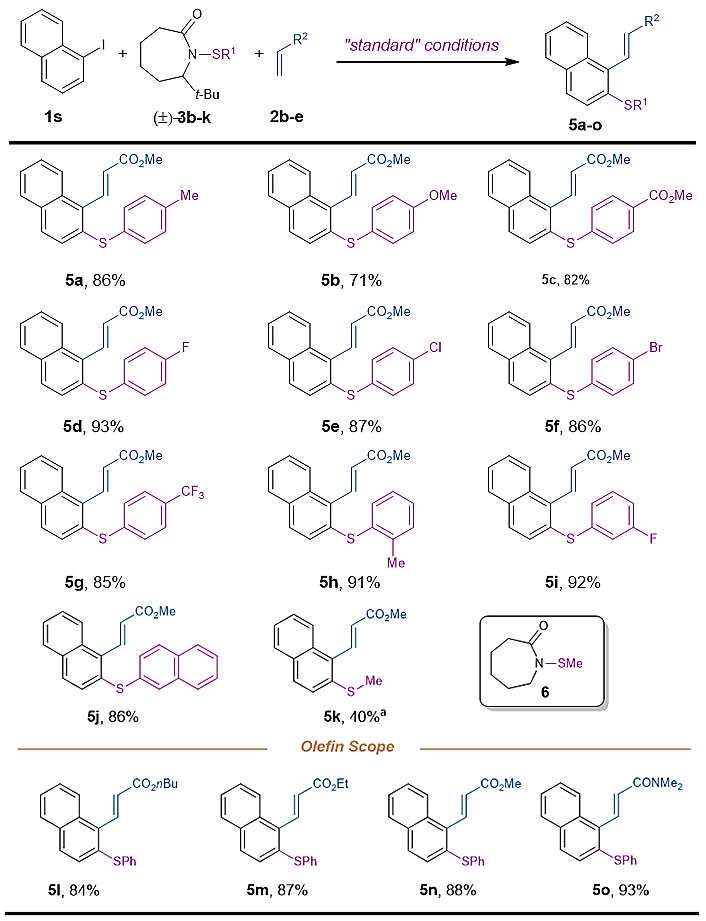
图5 硫试剂和烯烃底物拓展
作者还对该反应在合成方面的应用进行了考察。反应后产生的七元环内酰胺副产物能够以86%的收率被回收,它可以被用来重新制备硫酰胺亲电试剂(图6a)。该反应可以进行克级制备(图6b),反应产物可以通过选择性氧化反应制备亚砜和砜的衍生物(图6c)。在芳基的原位除了可以发生Heck反应、Suzuki以及Sonogashira偶联反应也取得了初步成果(图6d)。
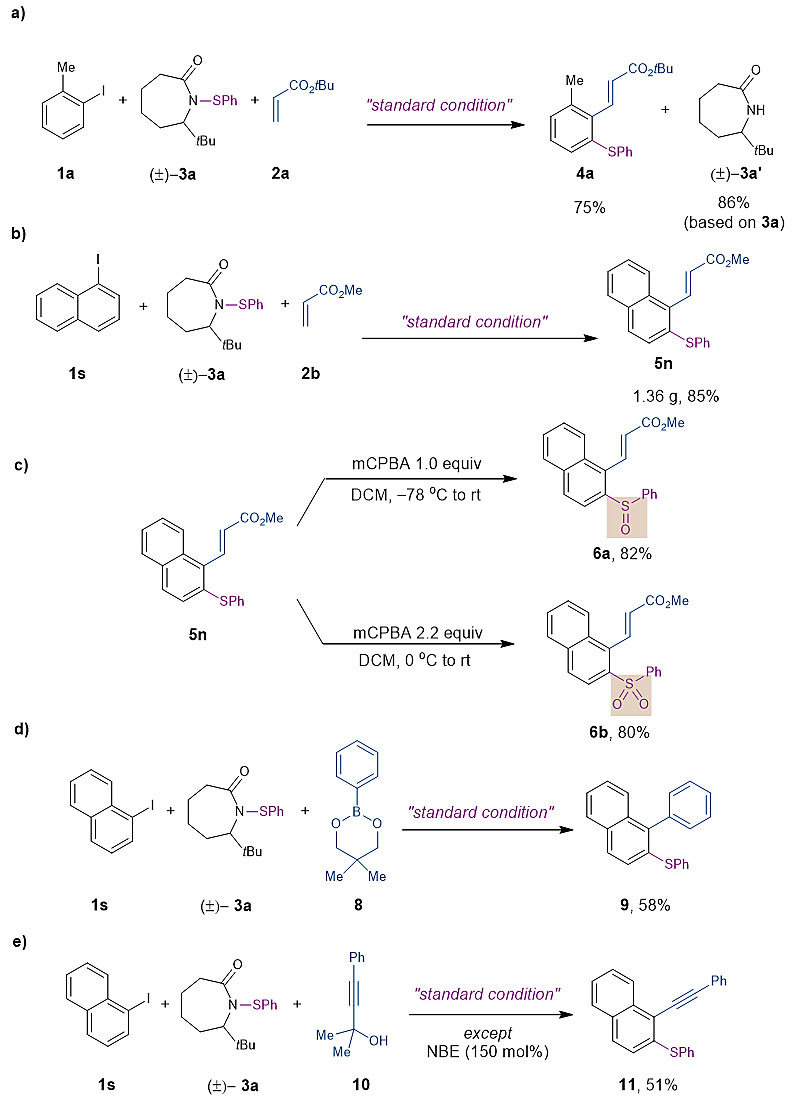
图6 合成应用
总结
董广彬课题组通过设计一种独特的亲电硫化试剂,实现了钯/降冰片烯协同催化碘苯的邻位硫化反应。该反应表现出了非常好的底物适应性与官能团兼容性,一系列芳基、稠环和杂环碘代物均可以参与转化。该反应广泛的官能团普适性和非常好的化学选择性使得其在复杂分子合成方面有着潜在的应用价值。
这一成果近期发表在Nature Communications上,Renhe Li 为文章的第一作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Sulfenamide-enabled Ortho Thiolation of Aryl Iodides via Palladium/Norbornene Cooperative Catalysis
Renhe Li, Yun Zhou, Ki-Young Yoon, Zhe Dong, Guangbin Dong
Nat. Commun., 2019, 10, 3555, DOI: 10.1038/s41467-019-11398-0
导师介绍
董广彬
https://www.x-mol.com/university/faculty/352
 0
0











