有机膦催化的Domino环化反应,由于其原子经济性、步骤经济性、反应条件温和以及操作简单的优点,受到化学家的青睐。联烯酸酯因其结构特殊性和反应形式多样性,被广泛用作环化反应的原料,已有许多开创性的工作相继报道,显示出了巨大的合成潜能。虽然在此领域取得了很大进展,开发联烯酸酯新的反应模式仍存在着较大的发展空间。
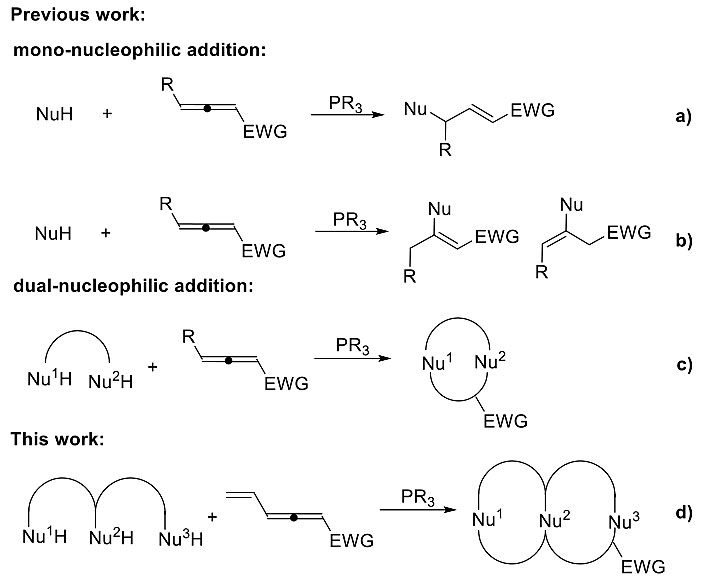
图1 有机膦催化的联烯酸酯的反应模式
近日,南开大学黄有教授(点击查看介绍)课题组报道了一种设计的新型联烯酸酯-γ-烯基取代联烯酸酯,实现了膦催化的三重亲核加成的(3+2)(2+3)连续环化反应,发展了一类高效合成氮杂多环化合物的新策略。相对于普通的联烯酸酯,γ-烯基联烯酸酯由于引入烯基,反应过程中面临一些挑战:反应位点多、竞争反应多、化学选择性和区域选择性控制难度加大。该团队通过设计合适的多位点亲核试剂,探索催化剂、温度等因素对反应的影响,找到了最优条件,可以高效的合成多环化合物,而且反应生成的两个非对映异构体可以通过柱层析分离得到,为Hydropyrroloimidazolones类天然产物的合成提供了新的思路。在最优条件下,该(3+2)(2+3)环化反应表现出良好的底物适用性。
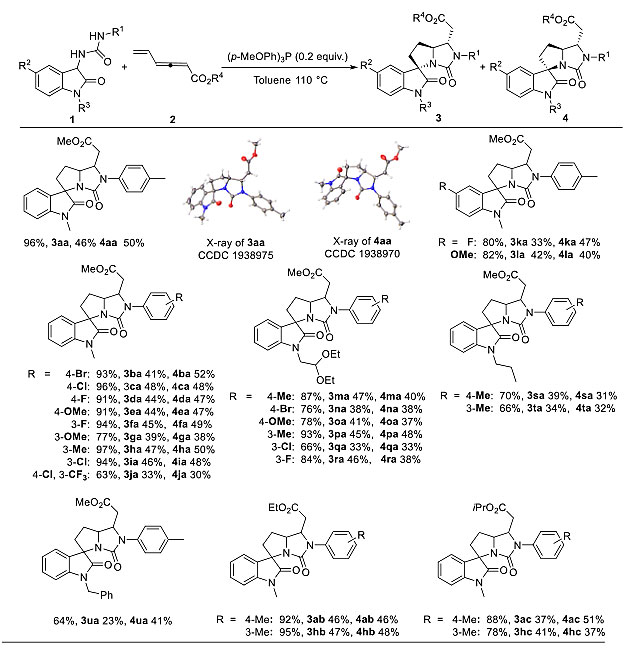
图2 多亲核试剂的适用范围
为了更好地理解反应机理,该研究团队进行了相关实验,通过分离反应中间体,同位素标记实验,结合同位素分布分析,提出了合理的反应机理。
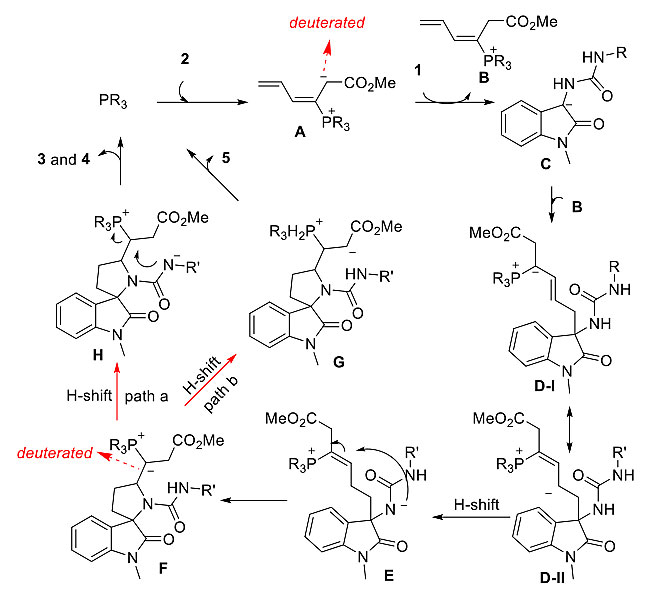
图3 反应机理
有趣的是,有多个反应位点的烯炔化合物也可以在此条件下实现(3+2)(2+3)环化反应,扩大了这一反应的应用范围。机理研究表明,在此反应过程中烯炔酸酯和γ-烯基联烯酸酯在膦催化下都会形成相同的反应中间体。
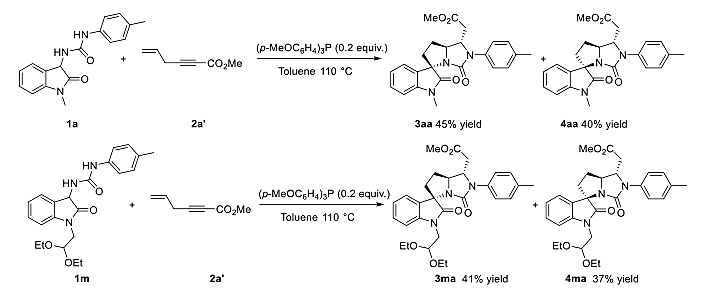
图4 烯炔参与的反应
综上,黄有教授课题组设计合成了γ-烯基联烯酸酯,通过三重亲核加成反应实现了与脲类底物的连续环化反应,通过设计新的联烯酸酯,引入了新的反应位点,进一步扩展了联烯酸酯的反应模式。该方法操作简便,反应条件温和,底物适用性强,为含氮杂环化合物的合成提供了新的路径。
相关工作发表在Chemical Communications 上,第一作者是冯佳旭博士。该研究工作得到了国家自然科学基金委(21672109, 21871148,21472097, 21172115,20972076),天津市自然科学基金(15JCYBJC20000 ,10JCYBJC04000 ,05YFJMJC00600)和南开大学的资助。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Phosphine-catalyzed (3+2)/(2+3) sequential annulation involving a triple nucleophilic addition reaction of γ-vinyl allenoates
Jiaxu Feng, You Huang
Chem. Commun., 2019, 55, 14011-14014, DOI: 10.1039/c9cc07346a
导师介绍

黄有教授简介
黄有,南开大学教授,博士生导师。1986年本科毕业于河南师范大学化学系,1997年于浙江大学化学系获得有机化学博士学位。1997-1999年,在南开大学元素所进行博士后工作(合作导师:陈茹玉院士),1999-2002年,在大阪大学药学院从事博士后研究(合作导师:Hidenobu Ohmori和Hatsuo Maeda)。2011年起,在南开大学化学院担任教授、博士生导师。黄有教授先后获得南开大学“敬业”奖教金教学二等奖,南开大学校级“教工先锋岗”先进个人,南开大学第五届“良师益友”提名奖等荣誉称号。课题组主要研究领域包括有机膦催化的Domino环化反应、硫叶立德参与的Domino环化反应、新型手性膦催化剂的设计合成及其不对称催化反应研究。目前,该课题组已经在Angew. Chem. Int. Ed., ACS Catal., Org. Lett., Chem. Commun., Chem. Eur. J. 等国际化学期刊发表论文90余篇。
http://www.x-mol.com/university/faculty/11847
http://skleoc.nankai.edu.cn/info/1018/1670.htm
https://hyou.scholar.group/?tdsourcetag=s_pcqq_aiomsg

博士研究生冯佳旭简介
冯佳旭,2011年考入延边大学,并于2015年获得理学学士学位。同年考入南开大学师从黄有教授攻读硕士学位,2017年转为博士研究生,从事有机膦催化反应研究。
 0
0