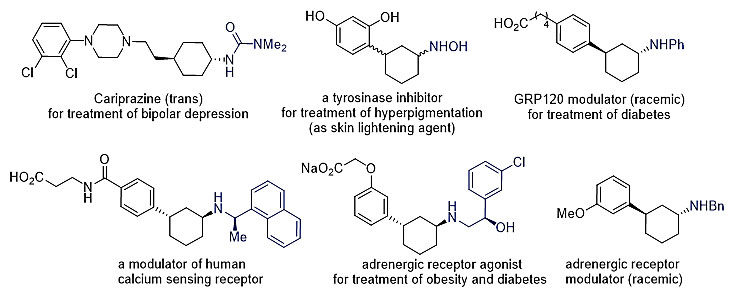
环己烷片段在药物分子中广泛存在,包括用于治疗抑郁症的cariprazine和刺激胰岛素分泌的glimepiride等药物分子。作为候选药物的核心骨架,胺化的环己烷结构在药物发现中正变得尤为重要。胺官能团的引入不仅有助于药物片段的组装,而且还能够提供与靶受体的氢键结合位点。环己烷上因胺化后引入的新立体中心,形成了独特的三维形状,有助于减少引起副作用的混杂结合,增加通过临床试验的成功几率。近期,北京大学深圳研究生院周建荣团队报道了一种高效不对称构筑该结构的方法。
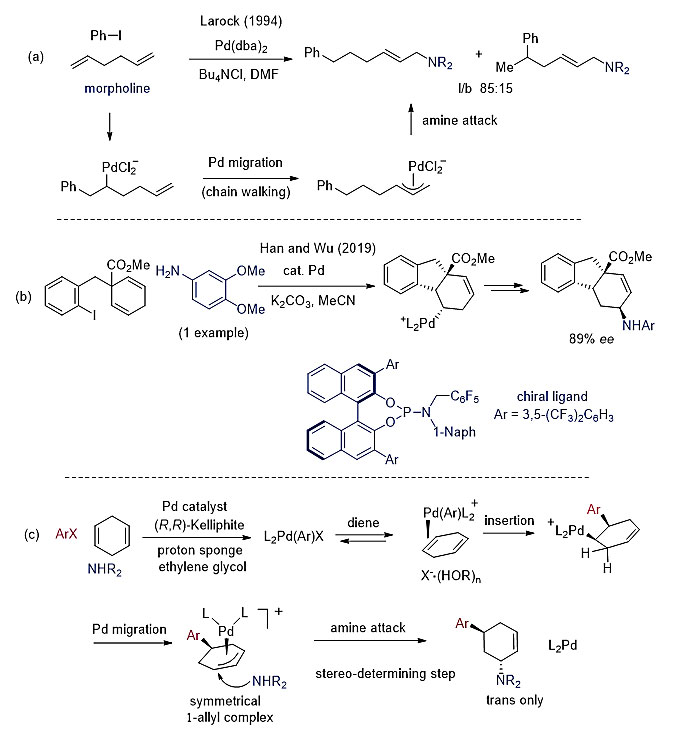
1990年代初,Larock小组就已经报道了非共轭二烯的Heck芳基化反应随后被亲核试剂捕获。但多年以来,非共轭二烯的不对称反应仍然没有突破性的进展。相比之下,共轭二烯的不对称Heck插入和亲电捕获却取得了很大的进展,如Shibasaki、龚流柱和韩志勇等课题组的贡献。2019年,吴祥等人发表了分子内1,4-环己二烯的不对称的Heck环化反应,随后被丙二酸酯,酚和一例特殊的芳胺捕获。由于在该反应中烯烃的插入是立体决定步骤,所以与分子间的Heck环化反应相比较易实现。
最近,周建荣团队首次报告了非共轭环状二烯的不对称三组分Heck芳基化/胺化反应。作者从商业可得的三种简单原料出发,同时实现了C-C 键和C-N键的构筑且单一选择性的完成了两个手性中心的构筑。
成功实现该反应主要有几个挑战:1)配体的选择非常关键,需要弱供电子的配体完成芳基碘插入反应的同时实现γ-位环烯丙基Pd络合物的手性诱导,而这种弱相互作用创造的手性环境极易被外加亲核试剂所破坏,导致ee值的降低。2)π-环烯丙基Pd的不对称胺化反应比较特殊,迄今仅有几例报道。3)胺捕获的步骤是可逆的,当使用三乙胺和二异丙基乙基胺作碱替代质子海绵时,延长反应时间,ee值出现了降低。
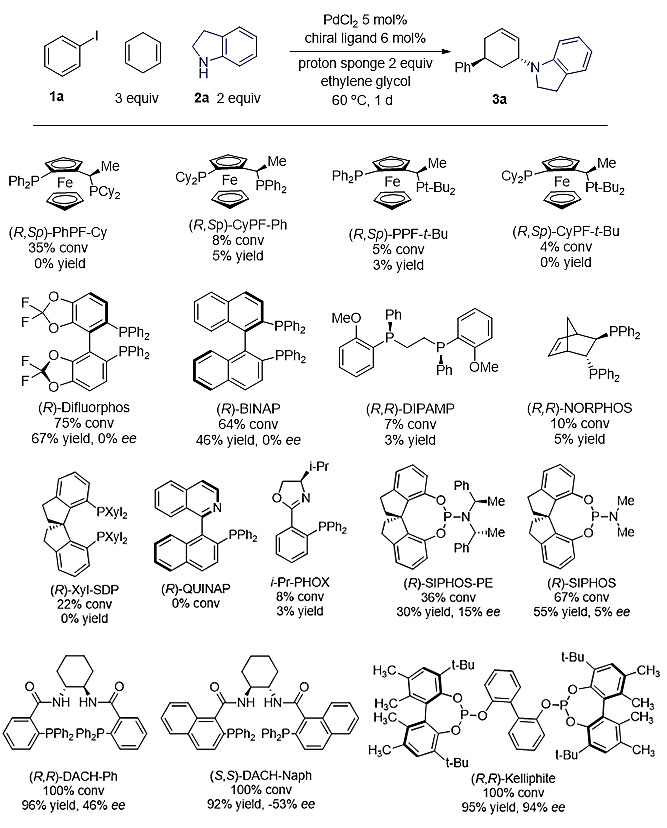
关于模板反应的选择,作者首先尝试了经典的苯基三氟甲基磺酸酯作为亲电试剂,但由于其在碱性条件下易水解,且反应活性较低,最终选择了活性较高且不会水解的碘苯。在碘苯、1,4-环己二烯和吲哚啉的模板反应中,通过大量的手性配体考察发现BINAP和Difluorphos可以得到很好的收率,但ee值为零。其他手性膦配体,包括Josiphos配体、DIPAMP、Norphos、PHOX和QUINAP表现的活性很低。手性磷酰亚胺配体可以得到中等的收率,但ee低于20%。通常情况下,Trost配体是Pd催化烯丙基不对称反应的优选,但在该反应中仅仅得到约50%ee。比较幸运的是,作者最终发现特殊的弱供电子Kelliphite可以得到很好的结果,该配体也是首次被成功用到不对称烯丙基化反应,打开了这类配体开发使用的空间。
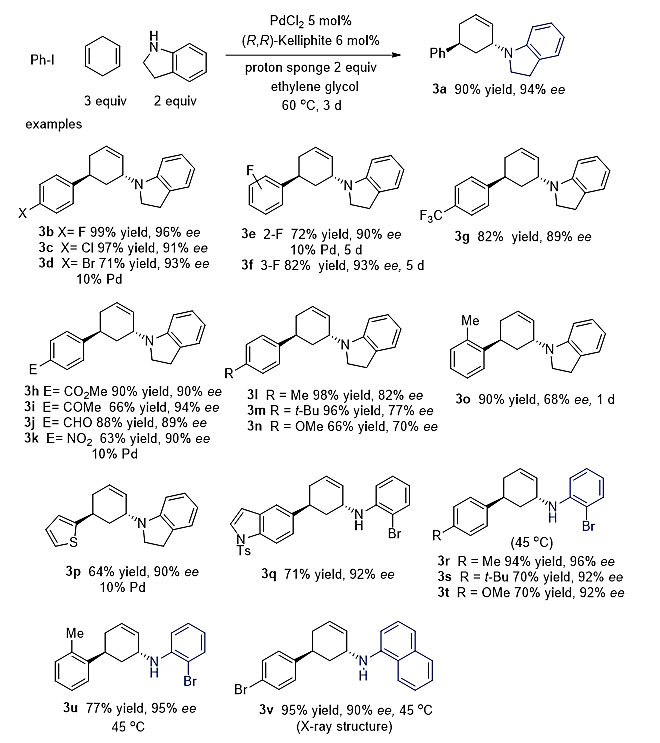
在摸索出最优条件之后,作者对芳基碘代物进行了考察,发现该反应对卤素F、Cl、Br均有很好的兼容性 (3b–3f),其他常见的官能团如酯基、羰基、醛基以及硝基在该反应体系中也均表现出很好的耐受性 (3h–3k)。供电子的基团会降低目标产物的ee值 (3l–3n),但当用大位阻的邻溴苯胺替代吲哚啉时,ee值有显著的提高 (3r–3t)。值得一提的是,该反应同样适用于富电子杂环芳烃如吲哚、噻吩等结构 (3p–3q),比较遗憾的是,缺电子吡啶杂环对该体系并不适用。该类产物的绝对构型最终由化合物3v晶体结构确定。
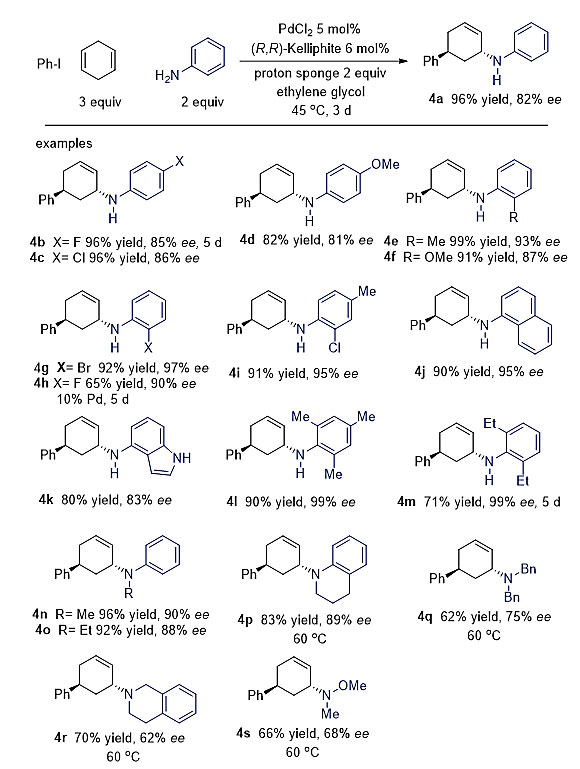
在完成芳基碘代物的考察之后,作者对胺亲核试剂进行了研究。对于芳香伯胺化合物而言,无论吸电子基或者供电子基团,反应均得到约80% ee的产物 (4b–4d)。当芳胺的邻位带有取代基时,产物得到了大于90% ee值 (4e–4i),当邻位有两个取代基时,由于位阻进一步增大,可以得到近乎光学纯的产物 (4e–4i)。此外,胺类底物除了可以容忍卤素基团还可以兼容吲哚NH官能团 (4k),芳香仲胺同样得到了很好的结果 (4e–4i)。令人高兴的是,其他胺类化合物如双苄胺、四氢异喹啉及羟胺也同样得到了不错的结果 (4q–4s);但不幸的是,其它烷基胺类化合物(四氢吡咯、二乙胺)以及杂芳环取代的胺(吡啶、嘧啶和苯并恶唑)由于可以与金属催化剂钯结合的原因,没有得到目标产物。
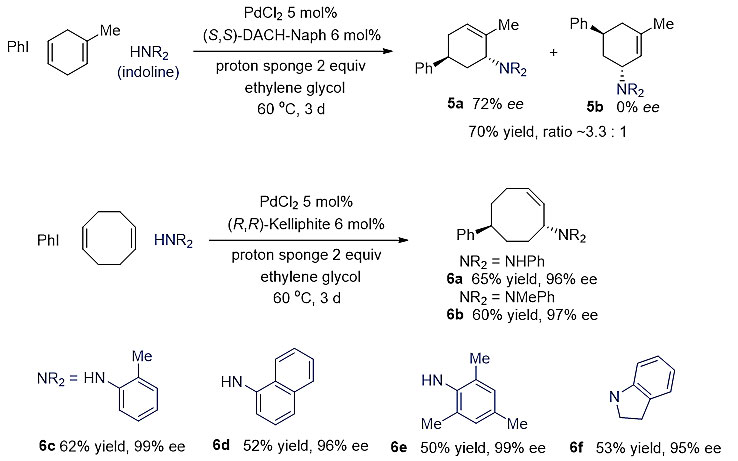
最后,作者对其它环烯烃进行了考察,发现最优条件在有取代的1,4-环己二烯的反应中得到了很低的ee值。发现只有Trost配体可以得到中等的收率和ee值。1,5-环辛二烯在标准条件下仍然得到了目标产物。由于产生Heck副产物,反应的收率有所降低,但各种芳香胺亲核试剂均可以得到非常好ee值。
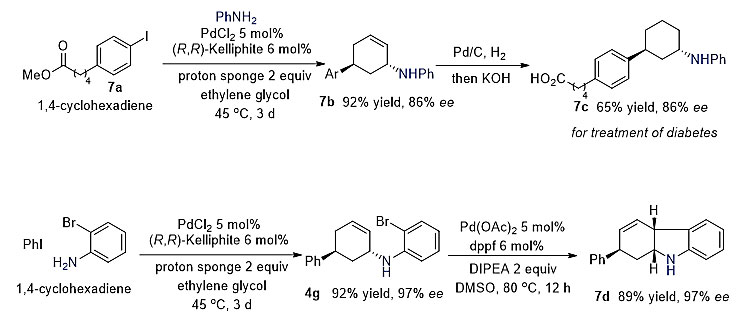
为了验证该合成方法的实用性,作者通过使用底物7a,得到产物7a,仅一步氢化反应即完成了可治疗糖尿病的活性化合物7c的合成。此外,以化合物4g为例,邻溴苯胺的产物可通过进一步的Heck反应转化为手性的四氢咔琳,该结构是许多药物分子的核心骨架,但目前已有的合成路线绝大多数都是消旋体合成。
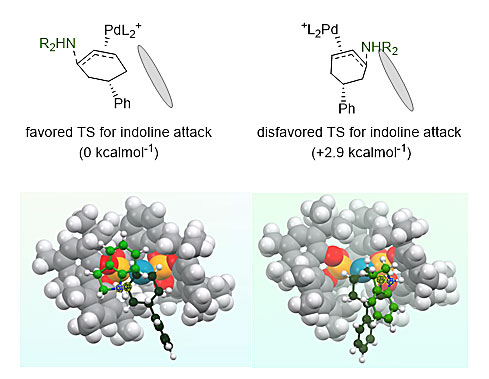
为了进一步理解该反应之所以有很好对映选择性,作者与黄国伟教授课题组合作,对反应路径进行了DFT计算,最后发现反应经历上图(左)的胺进攻历程能量较低。
综上所述,周建荣团队首次开发了非共轭环状二烯的三组份Heck芳基化/胺化反应,该反应具有单一的反式选择性和很好的对映选择性。经研究发现,弱供电子配体的Kelliphite起到至关重要的作用。一方面它活化经芳基插入和钯迁移形成的π-环烯丙基配合物,确保胺试剂亲核进攻的完成;另一方面它形成很深的手性口袋,从而完成远端反应位点的手性诱导,使得胺试剂从反面进攻,取得很好的对映选择性。
这一成果近期发表在Angew. Chem. Int. Ed. 上,第一作者朱道勇博士,2018年博士毕业于兰州大学,师从涂永强院士,现在新加坡南洋理工大学做博士后研究。通讯作者周建荣教授已于2019年离开南洋理工大学,开始全职在北京大学深圳研究生院工作。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Asymmetric Three‐Component Heck Arylation/Amination of Nonconjugated Cyclodienes
Daoyong Zhu, Zhiwei Jiao, Yonggui Robin Chi, Theo P. Goncalves, Kuo-Wei Huang, Jianrong Steve Zhou*
Angew. Chem. Int. Ed., 2020, DOI: 10.1002/anie.201915864
 0
0









