萜类 (terpenoids),又称类异戊二烯 (isoprenoids),约占所有天然产物的三分之一,是自然界存在种类最多的化合物,除了在细胞生理运作中扮演重要角色,萜类在医药、工业和生物技术等领域中更具有广泛的应用,胆固醇、胡萝卜素、紫杉醇、青蒿素、天然橡胶等,都是萜类化合物。所有萜类化合物都由五个碳原子的二甲基丙烯基焦磷酸 (dimethylallyl diphosphate,DMAPP) 和异戊烯基焦磷酸 (isopentenyl diphosphate,IPP),经不同萜类合成酶 (isoprenyl diphosphate synthase,IDS) 催化缩合反应而产生。根据产物碳键的立体构型,IDS可大致分为反式-萜类合成酶 (trans-IDS) 和顺式-萜类合成酶 (cis-IDS)。相较于trans-IDS,cis-IDS家族的蛋白质拥有更多变的活性区结构和更多样化的功能,由于结构类似展翅的蝴蝶,因此也称为“蝴蝶样折叠” (butterfly-fold)。湖北大学生命科学学院、省部共建生物催化与酶工程国家重点实验室的陈纯琪教授团队长期研究萜类合成酶结构和反应机理,尤其对多种新型cis-IDS基础研究作出重要贡献,近期与张丽兰博士、喻雪婧副教授、马立新教授 (院长及国重主任) 和郭瑞庭教授共同合作完成了cis-IDS的结构特征和催化机理研究的综述,内容将对研究生物合成重要的天然产物及医药中间体、细胞代谢和疾病控制等提供重要的理论指导。文章被ACS Catalysis选为“ACS Editors'Choice” (图1) 和封面文章 (Supplementary Cover) (图2),已在线刊出且免费开放。
图1. 文章获选为2020年4月9日的ACS Editors' Choice。ACS Editors' Choice入选率低于1 %,每一年, ACS的编辑们每年从4万多篇期刊论文中选取365篇优秀论文 (每日一篇) 放到ACS的首页上,作为ACS Editors' Choice,相当于每天的头条报道,并永久免费开放。

图2. 文章获选为ACS Catalysis 封面文章 (Supplementary Cover)。图中显示数个代表性蝴蝶样折叠酶晶体结构。
1. 同源二聚体cis-IDS:常规的“头-碰-尾”式缩合
典型的cis-IDS为同源二聚体,以“头-碰-尾”的缩合方式产生10-120个碳的线性产物。第一个发现的cis-IDS为来源于藤黄微球菌的十一异戊烯基焦磷酸合成酶 (undecaprenyl diphosphate synthase,UPPS),以十五个碳的法尼基焦磷酸 (farnesyl diphosphate, FPP) 为底物,连续缩合八个IPP形成五十五个碳的十一异戊烯基焦磷酸。UPPS的催化机理被研究的比较透彻,因此成为cis-IDS相关研究的模型和基准 (图3A-C)。和其它细菌只产生一种cis-IDS不同,肺结核杆菌利用两个cis-IDS来生产五十个碳的产物,首先是Rv1086缩合十个碳的牻牛儿基焦磷酸 (geranyl diphosphate, GPP) 与一个IPP,形成顺式构型的FPP产物 ((Z,E)-FPP)。接着Rv2361以(Z,E)-FPP为底物,连续缩合七个IPP生成十异戊烯基焦磷酸。十一异戊烯基焦磷酸跟十异戊烯基焦磷酸都跟细菌的细胞壁合成有关,所以UPPS, Rv1086与 Rv2361是新型抗生素的标靶。从晶体结构分析可看出,UPPS跟Rv2361c底物结合口袋两侧的螺旋结构富有弹性,因此可以容纳较大的产物,相对应的螺旋结构在产物较小的Rv1086中则展现较大的刚性,所以只能结合较短的产物 (图3D) 。

图3. 合成直链型的同源二聚 cis-IDS立体结构和催化反应机理。(A) 大肠杆菌UPPS与Mg2+、 IPP和硫代法尼基焦磷酸 (FsPP) 的复合体结构 (PDB ID,1X06)。同源二聚体的两个单体分别用“红色/黄色和蓝色/紫色”表示,S1和S2分别为两个活性口袋。(B) UPPS催化中心关键氨基酸与底物和金属离子互相作用,虚线表示距离小于3.5 Å。(C) UPPS的反应机理, D26为UPPS催化中心氨基酸。(D) 大肠杆菌UPPS、肺结核杆菌Rv2361和Rv1086晶体结构。红色标示α2和α3两个螺旋,中间形成的空间是S1底物结合区口袋。
2. 异源二聚体cis-IDS:长链直链型产物
长链聚萜类主要包括多元醇前体 (碳数80-100) 和天然橡胶 (碳数>10000)。多元醇是糖的脂质载体,负责携带糖转运到蛋白质上进行糖基化。天然橡胶是分子量最大的天然化合物,聚合物硫化橡胶广泛应用于各种产品。这两种长链的萜类合成酶是异源二聚体cis-IDS。其中,多元醇的催化单元早在几十年前就被鉴定出来,奇特的是这些在细胞中呈现膜相关的散布模式缺乏跨膜区。直到2011年才发现,这些酶其实需要一个具有跨膜区的伴侣蛋白质,生化与结构证据表明,这些伴侣蛋白质也采用蝴蝶状折叠,但是活性中心的几个特征都消失了,仅保留了与具有活性的单体形成二聚体的界面 (图4)。这些证据进一步展现了cis-IDS家族成员的多变。
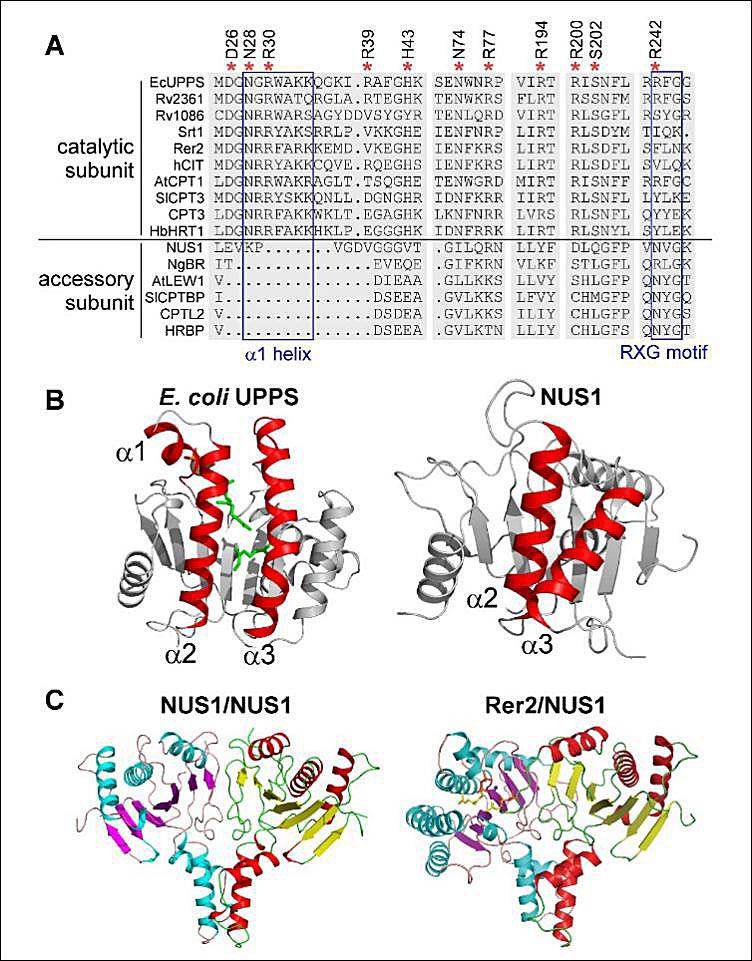
图4. 异源二聚体构型cis-IDS序列和结构特征。(A) 几个非催化cis-IDS单元的一级序列比对。(B) 大肠杆菌UPPS和非催化单元NUS1的单体结构。红色显示的两条α螺旋构成 S1底物结合区,NUS1的α3向内倾斜堵塞S1通道,底物结合区因而消失。(C) NUS1形成的同源二聚体 (左) 与模拟的NUS1和催化单元 (Rer2) 形成的异源二聚体 (右)。
3. 非典型 cis-IDS:非“头-碰-尾”式缩合
近来越来越多非直链型的萜类化合物被鉴定出来,它们具有广泛多样的生物活性,是化工产业和药物研发的重要前体。这些特殊萜类的生物合成过程常异于典型直链萜类,大部分是由cis-IDS家族成员催化合成的。第一个支链型cis-IDS是熏衣草焦磷酸合成酶 (lavandulyl diphosphate synthase,LPPS),LPPS催化两分子DMAPP缩合生成熏衣草精油前体LPP (图5A)。熏衣草精油是一种天然香料,由熏衣草提炼而成,有护肤、降血压、安抚心悸和帮助睡眠等功效。来源于链霉菌的CLDS是衣草花青菌素前体合成酶,此类化合物具有抗肿瘤,保护神经元细胞,抗感染等活性。CLDS和LPPS一样也缩合两个DMAPP反应生成LPP,不同的是CLDS会紧接着使LPP环化 (图5A)。CLDS和LPPS的底物结合模式相当类似,但CLDS的S2底物结合口袋更窄,因而造成环化的发生 (图5B)。

图5. LPPS和CLDS催化反应机理。(A) LPPS和CLDS催化两分子DMAPP的反应过程。(B) LPPS和CLDS复合体结构中,活性区关键氨基酸与底物类似物相互作用网络 (绿色:LPPS复合体结构; PDB ID,5HC8;蓝色: CLDS复合体结构; PDB ID,5YGK)。
更特别的底物结合区变化发生在来源于链霉菌的Mcl22,Mcl22以GPP和DMAPP为底物,催化头-碰-中的缩合反应产生ISLPP (图6A)。ISLPP 是 merochlorins前体,这一类杂萜天然产物对于抗甲氧西林的金黄色葡萄球菌具有很高的活性。典型的cis-IDS中的S1底物结合区存在于α2和α3之间的通道,而在Mcl22中,这个通道被几个较大氨基酸堵塞,GPP转而结合在一个位在蛋白质表面的通道里 (图6B)。这种底物结合模式的改变非常剧烈,显示了cis-IDS家族成员利用活性区的改变来产生各种催化反应。

图6. Mcl22催化反应机理和立体结构。(A) Mcl22催化GPP和DMAPP缩合反应产生ISLPP。(B) 大肠杆菌UPPS (EcUPPS,PDB ID,1X06)和Mcl22 (PDB ID,5XK9) 晶体结构,红色标记α2和α3螺旋形成的S1底物结合口袋 (黄色),最右方显示位于Mcl22表面的GPP底物结合位置。
还有更多的特殊cis-IDS成员,比如来源于肺结核分枝杆菌的Rv3378c可以缩合二萜tuberculosinyl diphosphate和腺苷,产物1-tuberculosinyladenosine可以保护细菌在人体内不受免疫细胞杀伤。Rv3378c的存在并不直接影响细菌的复制与生长,却与能否成功感染宿主有关,所以 Rv3378c是肺结核杆菌的毒力因子 (virulence factor)。有趣的是,Rv3378c、Rv1086和 Rv2361都具有相同的关键活性位点,而Rv1086跟Rv2361的抑制剂也能够抑制Rv3378c的活性,因此针对这一类cis-IDS成员设计抑制剂,有可能作为新型抗结核病的药物。
综合以上可知,cis-IDS家族成员的底物结合区变化非常多,能够催化各式各样典型和非典型的萜类合成反应,随着越来越多萜类被鉴定出来,可以预见的是将有更多此家族成员会被发现,而这一群蛋白质就像是展翅飞舞的蝴蝶一样,各自展现着不同的型态以丰富天然化合物的多样变化。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Versatile cis-isoprenyl Diphosphate Synthase Superfamily Members in Catalyzing Carbon–Carbon Bond Formation
Chun-Chi Chen*, Lilan Zhang, Xuejing Yu, Lixin Ma, Tzu-Ping Ko, Rey-Ting Guo*
ACS Catal., 2020, 10, 4717-4725, DOI: 10.1021/acscatal.0c00283
 0
0