恶性黑色素瘤是一种罕见癌症,在日本每10万人中约有1~2人罹患此病,不仅是皮肤,还会出现在眼球、鼻腔、口腔及食道等粘膜上。如果恶性黑色素瘤仅发生在皮肤和粘膜上,可以通过外科手术切除病变部位及其周围组织进行治疗。但如果生长在脸部和头颈部,则会严重损害这些部位的功能和姿容,多数情况都难以通过外科手术治疗,而是结合放疗和抗癌药等进行治疗。另外,如果已经转移到淋巴结和其他器官,则需要结合外科手术、放疗和抗癌药等药物疗法进行治疗,但以往的放射疗法难以生效,预后较差,需要开发新的治疗方法。近年来,通过免疫检查点抑制剂和分子靶向药物提高疗效的方法被看好,但研究发现,这两种方法针对恶性黑色素瘤均有不足,而且医疗效果也因人而异。近年来,靶向核素治疗成为了一种治疗效果优异、安全系数高、毒副作用小的癌症治疗方式。目前,美国食品药品监督管理局(FDA)已经批准一种名为Lutathera(lutetium 177 dotatate)用于治疗神经内分泌肿瘤。研究人员认为开发针对恶性黑色素瘤的靶向核素药物可以克服传统疗法的不足,并且对于小的转移病灶可以实现有效治疗。
近日,日本国立研究开发法人量子科学技术研究开发机构(以下简称“量研”)的研究人员利用量研自有的加速器成功制造了放射性核素211At(砹-211)。221At是一种半衰期为7.2 小时的放射性核素,其可以释放射程为几个细胞直径之和的的α射线,这些射线会对命中的细胞进行杀伤破坏。因此,如果能将211At有效地送到癌细胞中,则有望做到在不损害周围正常组织的情况下治疗癌症。为了开发靶向递送211At的药物分子,研究人员瞄准了高密度存在于癌细胞表面的蛋白质——代谢型谷氨酸1型受体(mGluR1)。已有文献报道表明mGluR1存在于恶性黑色素瘤和乳腺癌等多种癌细胞的表面,与癌症的形成和生长密切相关。因此,mGluR1有望成为开发癌症诊断和治疗药物的靶标。张明荣教授课题组数年前就开始了针对mGluR1的核医学影像分子的开发。目前该课题组已成功开发出多种靶向mGluR1的正电子发射断层显像(PET:Positron Emission Tomography)药物(18F和11C标记的小分子诊断药物)。利用这些药物,成功对活体动物的癌细胞实施了PET成像(图1)[1,2]。
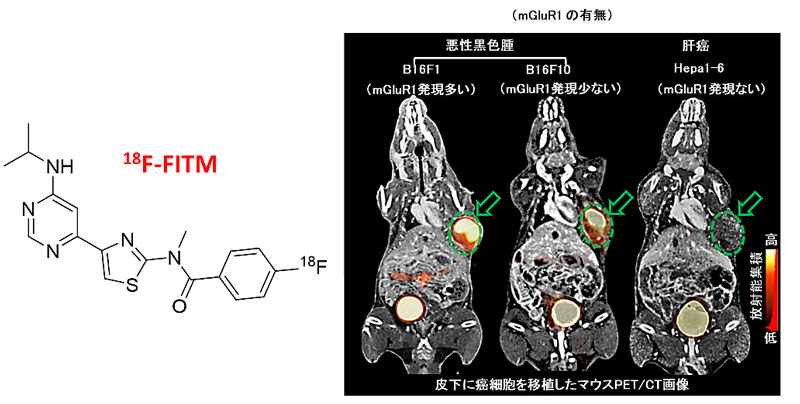
图1. 使用18F-FITM对mGluR1进行PET成像。
本研究利用此前开发与mGluR1结合的化合物,结合多年放射性药物开发积累的技术和临床试验经验,新开发了与mGluR1结合并释放α射线的新型靶向同位素治疗候选药物211At-AITM(4-211At-astato-N-(4-(6-(isopropylamino)pyridine-4-yl)-1,3-thiazol-2-yl)-N-methylbenzamide)(图2),并利用模型小鼠,评价了针对恶性黑色素瘤的抑癌效果。
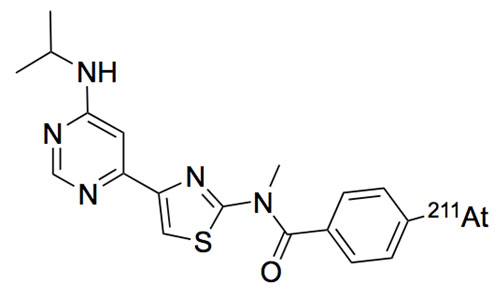
图2. 211At-AITM的结构式。
研究人员首先合成了与mGluR1强力结合的低分子化合物ITM(N-(4-(6-(isopropylamino)pyrimidin-4-yl)-1,3-thiazol-2-yl)-N-methylbenzamide),随后,成功对ITM 进行了211At标记,最终得到了211At-AITM。随后,研究人员向皮下移植了恶性黑色素瘤细胞的模型小鼠静脉注射一次211At-AITM,记录了肿瘤尺寸的变化。最终确认,分别注射1.11 MBq、1.85 MBq和2.96 MBq的211At-AITM的群组,与没有注射211At-AITM的群组相比,均显著抑制了癌细胞的繁殖(图3)。在注射2.96MBq的211At-AITM的群组,部分小鼠的肿瘤完全消失。另一方面,注射211At-AITM的所有群组均未观察到诸如体重减轻等副作用。
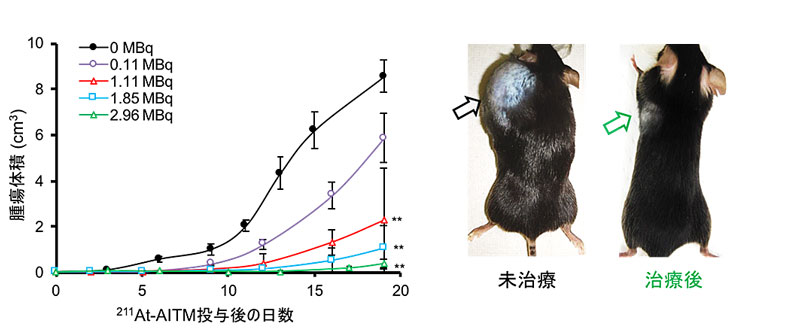
图3. 通过注射211At-AITM抑制癌细胞繁殖的效果比较。
基于上述结果,该课题组正在探究211At-AITM对其他高表达mGluR1肿瘤和转移瘤的治疗效果。研究人员表示,目前他们正在对该药物进行进一步优化,乐观估计,该药物有希望在未来几年推向临床。上述成果于近日发表在美国核医学会的核医学权威期刊Journal of Nuclear Medicine 。文章的共同第一作者量研量子医学医疗部门放射线医学综合研究所(以下简称“放医研”)先进核医学基础研究部的主任研究员谢琳和研究员破入正行,论文的通讯作者是放医研先进核医学基础研究部部长张明荣教授。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

131I-IITM and 211At-AITM: Two Novel Small-molecule Radiopharmaceuticals Targeting Oncoprotein Metabotropic Glutamate Receptor 1
Lin Xie, Masayuki Hanyu, Masayuki Fujinaga, Yiding Zhang, Kuan Hu, Katsuyuki Minegishi, Cuiping Jiang, Fuki Kurosawa, Yukie Morokoshi, Huizi Keiko Li, Sumitaka Hasegawa, Kotaro Nagatsu, Ming-Rong Zhang
Journal of Nuclear Medicine, 2019, DOI: 10.2967/jnumed.119.230946
参考文献:
1. Xie, L., Yui, J., Fujinaga, M., Hatori, A., Yamasaki, T., Kumata, K., Wakizaka, H., Furutsuka, K., Takei, M., Jin, Z.-H., Furukawa, T., Kawamura, K., and Zhang, M.-R. (2014) Molecular imaging of ectopic metabotropic glutamate 1 receptor in melanoma with a positron emission tomography radioprobe 18F-FITM, International Journal of Cancer,135, 1852-1859.
2. Fujinaga, M., Xie, L., Yamasaki, T., Yui, J., Shimoda, Y., Hatori, A., Kumata, K., Zhang, Y., Nengaki, N., Kawamura, K., and Zhang, M.-R. (2015) Synthesis and Evaluation of 4-Halogeno-N-[4-[6-(isopropylamino)pyrimidin-4-yl]-1,3-thiazol-2-yl]-N-[11C]methylbenzamide for Imaging of Metabotropic Glutamate 1 Receptor in Melanoma, Journal of medicinal chemistry 58, 1513-1523.
 0
0












