化学动力治疗(Chemodynamic Therapy, CDT)是一种新兴的肿瘤治疗手段。CDT基于特殊的催化或类芬顿(Fenton-like)反应,将肿瘤微环境中较高含量的内源性过氧化氢转化为活性氧(Reactive Oxygen Species, ROS),从而破坏肿瘤组织。但由于肿瘤内过氧化氢含量有限、癌细胞有着较强的抗氧化修复机制,单一的CDT疗法无法彻底根除肿瘤。因此,CDT与其他疗法整合的协同诊疗手段亟待开发。
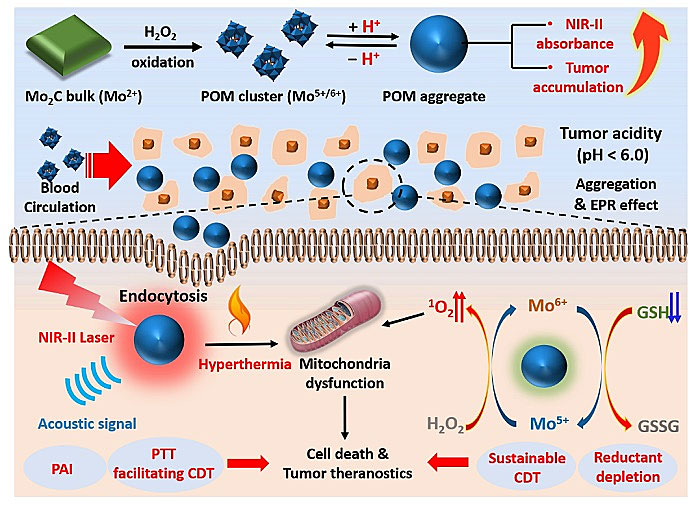
图1. POM制备过程以及作用机理
除现有的纳米CDT系统外,基于多金属酸簇(polyoxometalate, POM)的类芬顿体系也被认为具有优异的潜在CDT应用价值。而基于Mo元素的POM因能够对肿瘤内的还原性物质以及微酸性进行响应而被广泛应用于肿瘤特异性光声成像介导的光热治疗研究,但其氧化过程及潜在的CDT性能鲜有报道;而且现有相关研究均在近红外第一窗口(NIR-I)进行操作,不利于深层肿瘤治疗。
近日,南京工业大学董晓臣教授和黄维院士团队与新加坡南洋理工大学Chen Peng教授、南方科技大学奚磊教授合作,开发了一种以β-Mo2C为原料、绿色高效制备Mo基POM的新方法,揭示了其在肿瘤微环境下的氧化还原循环行为,并成功应用于第二近红外窗口(NIR-II)光声成像介导的光热、化学动力协同治疗。
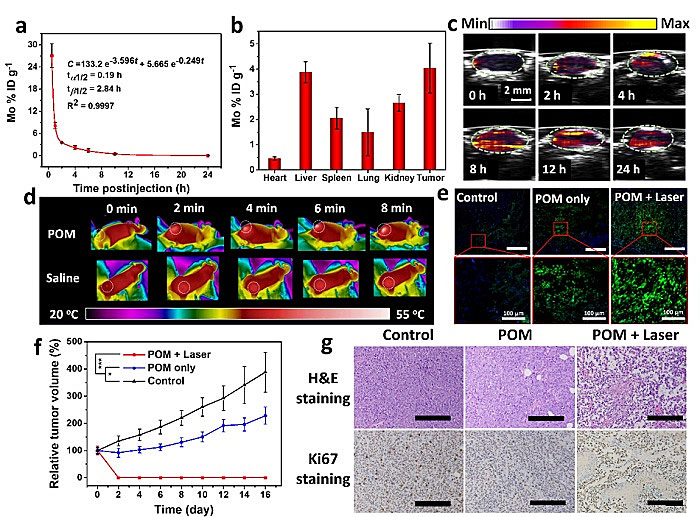
图2. POM在小鼠活体模型上的肿瘤诊疗性能
将微米级Mo2C块体进行一步氧化可大量高效制备POM纳米簇。POM纳米簇在中性条件下具有小于10 nm的粒径,而一经酸化(pH 6.5至pH 4.5),POM纳米簇会迅速聚集形成尺寸约100 nm的颗粒,且在NIR-II区域的光学吸收、光热转化能力大幅增强,该性质有利于其在肿瘤酸性环境中的富集与肿瘤特异性的光声成像。在被H2O2氧化过程中,POM中Mo元素由5价转化为6价,并通过POM特殊结构辅助下的Russell Mechanism途径产生具有细胞毒性的单线态氧(1O2)。同时,被氧化的POM能够消耗细胞内的还原性物质(例如谷胱甘肽),一方面减弱细胞的抗氧化修复,增强CDT效果;另一方面POM再次回归具有高光学吸收性能的还原态,实现持续治疗。
随后,研究者在细胞、活体肿瘤模型层面分别验证了POM基于氧化还原循环的CDT性能。在肿瘤微环境中,POM能够发挥优异的NIR-II光声成像功能,在非光照条件下单一的CDT治疗能在初期抑制肿瘤生长,但在光照条件下,肿瘤可被光热、化学动力协同治疗根除,且无复发。
相关结果发表于Angewandte Chemie International Edition,论文第一作者为南京工业大学硕士研究生刘功远。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Mo2C-Derived Polyoxometalate for NIR-II Photoacoustic Imaging-Guided Chemodynamic/Photothermal Synergistic Therapy
Gongyuan Liu, Jiawei Zhu, Heng Guo, Aihui Sun, Peng Chen*, Lei Xi*, Wei Huang, Xuejiao Song*, Xiaochen Dong*
Angew. Chem. Int. Ed., 2019, DOI: 10.1002/anie.201910815
导师介绍
董晓臣
https://www.x-mol.com/university/faculty/27732
黄维
https://www.x-mol.com/university/faculty/27680
Chen Peng
https://www.x-mol.com/university/faculty/45901
(本稿件来自Wiley)
 0
0












