近年来,过渡金属催化的卡宾交叉偶联反应已经成为有机合成化学中的一种适用范围广而又高效简洁的新方法,它为碳碳键的构筑提供了新的合成思路。在这些交叉偶联反应中,重氮化合物以及N-对甲苯磺酰腙是最普遍使用的金属卡宾前体,涉及这类重氮卡宾前体的偶联反应已经得到了较为深入和系统的研究。尽管如此,新型非重氮金属卡宾前体的开发以及它在交叉偶联反应中的应用依旧是有机合成化学领域中的一项重大的挑战并且具有重大的科学意义,尤其是当传统的金属卡宾前体无反应活性、化学结构不稳定、或者难以通过现有方法合成时等等。因此,基于之前对金属卡宾反应和硫代酰胺底物的研究,华侨大学宋秋玲教授(点击查看介绍)课题组报道了钯催化的硫脲或者硫代酰胺的Suzuki-Miyaura交叉偶联反应。
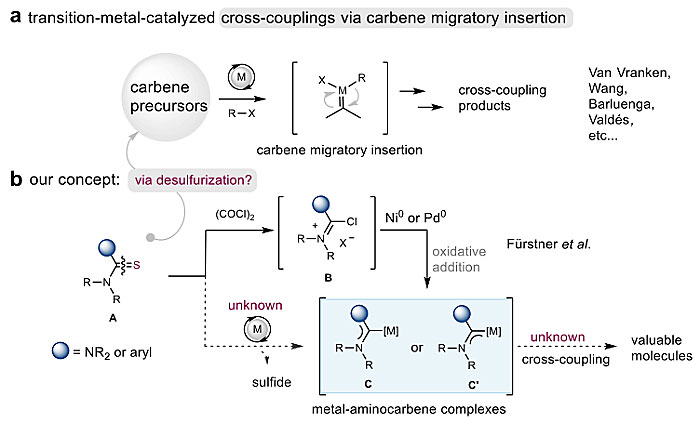
图1. 金属卡宾偶联反应与脱硫作用
该反应是基于金属卡宾的交叉偶联反应,具有相对容易放大、底物普适性广以及对水和空气都不敏感等优点,可以合成一系列取代的脒盐或者非对称芳基酮,其可能的反应机理是:首先,硫脲或者硫代酰胺在钯催化以及银盐的促进下发生脱硫作用,催化地形成钯氨基卡宾中间体,该中间体随后会与芳基硼酸发生转金属作用以及还原消除得到交叉偶联产物。值得一提的是,作者在研究反应机理的过程中合成并分离得到了钯氨基卡宾复合物的中性形式,并利用XRD单晶衍射分析确定了它的结构(图2);此外,作者还通过高分辨质谱分析证明了钯氨基卡宾复合物的阳离子形式的存在。机理研究还表明,银盐在该反应中起着双重的作用。
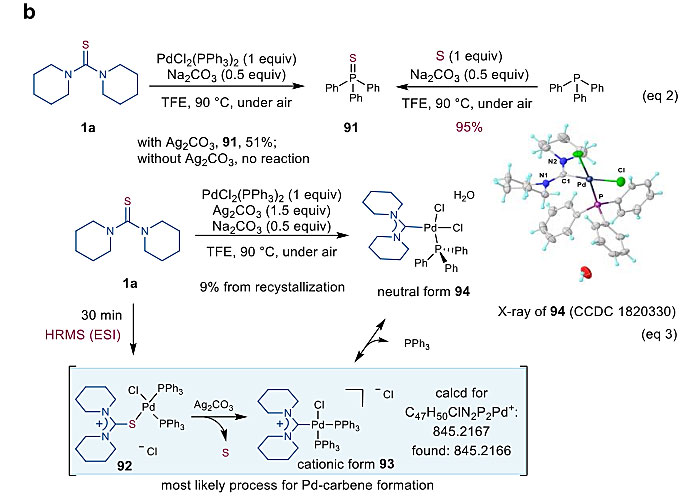
图2. 机理研究
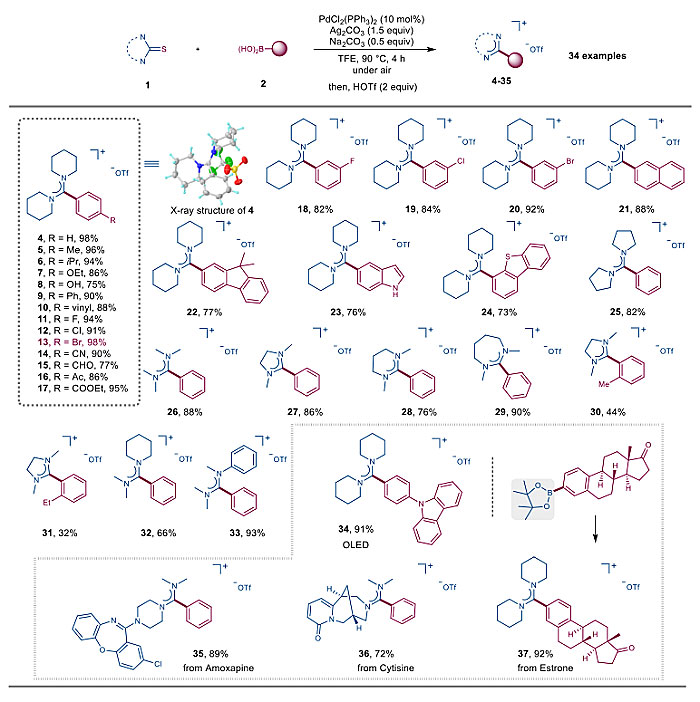
图3. 脒盐的底物范围

图4. 二芳基酮的底物范围
通过该方法可以合成一系列的脒盐类化合物(图3)和非对称的二芳基酮(图4)。在合成应用上,该方法可以实现放大反应,并且可以实现药物分子或天然产物的后修饰或合成,还可以从芳基硼酸出发合成氘代芳基甲醛等(图5)。该工作的发现,标志着硫脲或者硫代酰胺可以作为金属卡宾前体参与过渡金属催化的反应,并极大地丰富了硫脲化学。
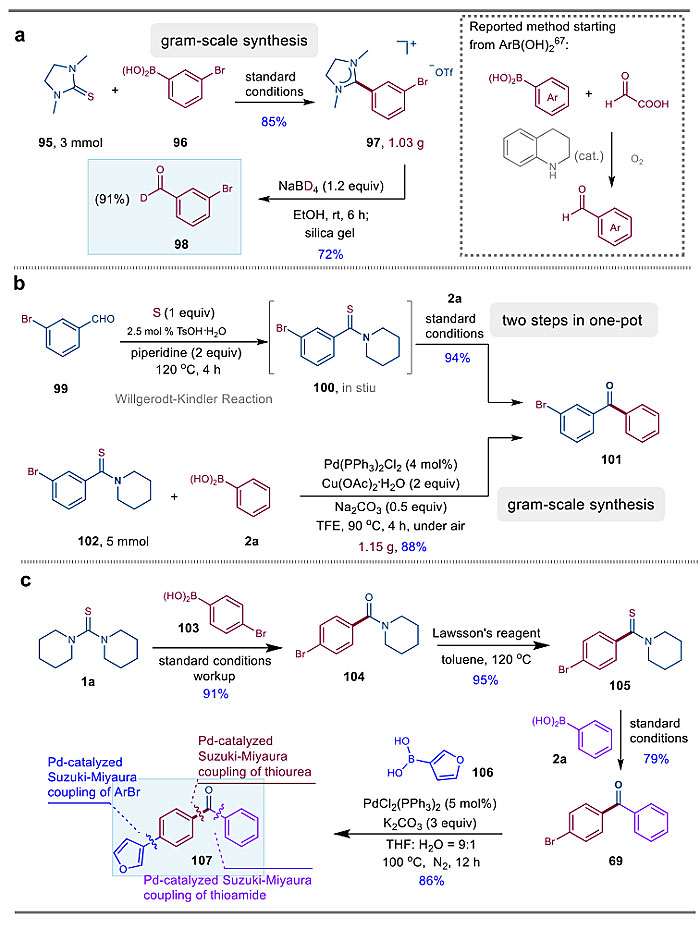
图5. 合成应用
相关工作发表在Nature Communications 上,上述研究得到国家自然科学基金和福建省自然科学基金的大力支持。第一作者为2016级博士麦少瑜。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Palladium-catalyzed Suzuki-Miyaura coupling of thioureas or thioamides
Shaoyu Mai, Wendong Li, Xue Li, Yingwei Zhao, Qiuling Song
Nat. Commun., 2019, 10, 5709, DOI: 10.1038/s41467-019-13701-5
导师介绍
宋秋玲
https://www.x-mol.com/groups/song_qiuling
 0
0









