英文原题:Macrocycle-Based Polymer Nanocapsules for Hypoxia-Responsive Payload Delivery
通讯作者: Ruibing Wang(王瑞兵)
作者:Chen Sun(孙臣), Ludan Yue(岳鲁丹), Qian Cheng(成谦), Ziyi Wang(王紫一),Ruibing Wang(王瑞兵)
细胞和组织乏氧是多种疾病的典型特征,尤其是实体肿瘤。这种局部缺氧的病理状态,常会破坏细胞的正常氧化还原水平,导致还原性应激增强。因此,利用正常组织和乏氧病灶之间生物还原酶水平的不同,多种基于乏氧响应的生物探针、前药和纳米载体等受到了科学家们的广泛关注。但已报道的众多乏氧响应纳米药物载体,普遍存在合成工艺复杂以及表面修饰繁琐等问题,极大程度上限制了其在生物医药领域的应用。
近日,针对这一问题,澳门大学中华医药研究院王瑞兵教授(点击查看介绍)团队设计并首次报道了基于大环分子共价键自组装的乏氧响应高分子纳米胶囊(NCs),并对其药物靶向递送以及乏氧响应释放进行了研究。通过简单的一步烷基化取代反应将具有双反应位点的乏氧响应性分子(BBA)与全羟基六元瓜环(PerhydroxyCB[6])交联成二维聚合物,将其置于水中可自组装形成空心纳米胶囊,药物分子可在自组装过程中负载到纳米胶囊中。同时,可通过六元瓜环(CB[6])和精胺(Spermine,SP)之间的主客体作用对纳米胶囊表面进行功能化修饰,如通过简单插入精胺修饰的叶酸(FA-SP)可得到靶向递药且乏氧响应的纳米胶囊(FA-SP/AZO-NCs,图1)。
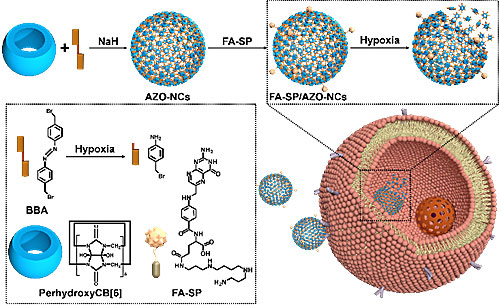
图1. FA-SP/AZO-NCs的制备以及乏氧响应示意图
在此工作中,该团队首先制备了AZO-NCs并通过扫描电镜(SEM)和透射电镜(TEM)对其进行了形貌表征。同时,对AZO-NCs在体外乏氧环境中的响应速率及粒子粒径变化进行研究,证明了在乏氧状态下,纳米胶囊会很快发生碎裂,继而碎片聚集。相较于AZO单体,AZO-NCs表现出更灵敏的乏氧刺激响应性,这是由于AZO-NCs具有更大的比表面积。接下来,针对FA-SP/AZO-NCs的特异细胞靶向递送能力进行了定性及定量研究,证明了AZO-NCs具有较好的生物相容性和稳定性。
为了验证AZO-NCs在细胞内乏氧条件下的响应性释放能力,该课题组利用共聚焦显微镜观察了摄取负载尼罗红染料的AZO-NCs的多种细胞,在以物理手段构建的梯度乏氧环境下,AZO-NCs在肿瘤细胞中表现出明显的释放效果。而在正常细胞中,由于其中较低的还原酶水平,AZO-NCs几乎不释放尼罗红(图2)。
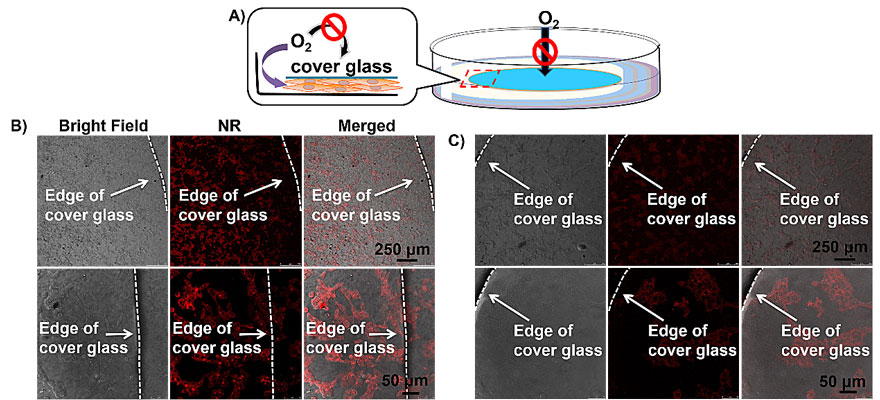
图2. A)乏氧细胞模型示意图;B)乏氧条件下,AZO-NCs在肿瘤细胞中释放染料,C) 乏氧条件下,AZO-NCs在正常细胞中几乎不释放染料。
最后,该课题组利用斑马鱼构建乏氧响应的体内模型,观察在斑马鱼体内AZO-NCs释放尼罗红的情况。与正常氧气环境下的斑马鱼对比,在乏氧环境中,斑马鱼的节段间血管和后主静脉中表现出明显的红色荧光(图3)。

图3. 在正常氧气环境及乏氧环境下,斑马鱼体内AZO-NCs释放荧光染料的情况。
本研究首次报道了基于大环分子共价键聚合的乏氧响应性纳米胶囊,通过主客体作用在纳米胶囊表面修饰靶向分子后,对该体系的靶向递送能力、乏氧响应释放能力进行了体外及体内研究。该研究为基于大环分子为构筑单元的响应性药物递送系统的纳米医学提供了崭新的设计思路。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Macrocycle-Based Polymer Nanocapsules for Hypoxia-Responsive Payload Delivery
Chen Sun, Ludan Yue, Qian Cheng, Ziyi Wang, Ruibing Wang*
ACS Materials Lett., 2020, DOI: 10.1021/acsmaterialslett.0c00002
Publication Date: February 12, 2020
Copyright © 2020 American Chemical Society
导师介绍
王瑞兵
https://www.x-mol.com/university/faculty/45874
(本稿件来自ACS Publications)
 0
0