在光动力治疗(PDT)过程中,光敏剂受光激发后,将三重激发态的能量转移给分子氧使其转化为强氧化性的单线态氧,诱发细胞凋亡促使肿瘤消融。激活型光敏剂(aPS)可被设计成仅在特定肿瘤标志物或肿瘤微环境下被激活,从而有效规避对正常组织以及皮肤的光损伤,进而提升光动力治疗的精准性。如何最大程度降低甚至彻底抑制激活前aPS的光毒性对规避非特异性光损伤至关重要。与此同时,促进aPS在目标病灶被快速激活并发挥高效的光敏作用是实现精准光动力治疗的另一关键。
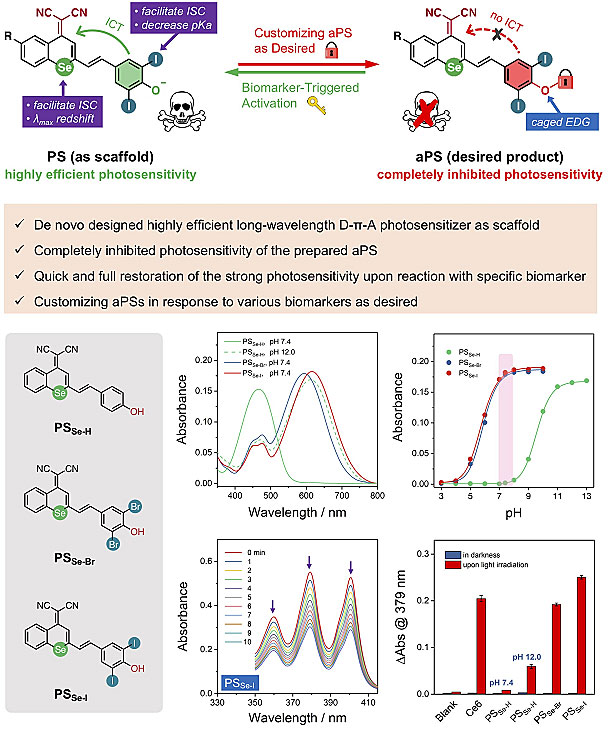
近日,南开大学李昌华教授(点击查看介绍)团队成功开发了一类全新的激活型光敏剂的制备方案,实现了光敏性能从彻底抑制到应激开启的激烈转变。这类激活型光敏剂以硒和碘取代的D-π-A型光敏剂(PSSe-I)为制备骨架,硒和碘通过重原子效应赋予了PSSe-I高效的光敏性能(约为商品化光敏剂Ce6的1.2倍)。更重要的是,硒元素进一步促进了光敏剂吸收峰的显著红移(相对于氧代类似物红移约70纳米),这将有效提升光动力治疗光源的组织穿透深度;而碘元素的引入则有效降低了酚羟基的pKa(由9.66降低至5.78),使得PSSe-I在生理pH条件下保持最优的光敏性能。
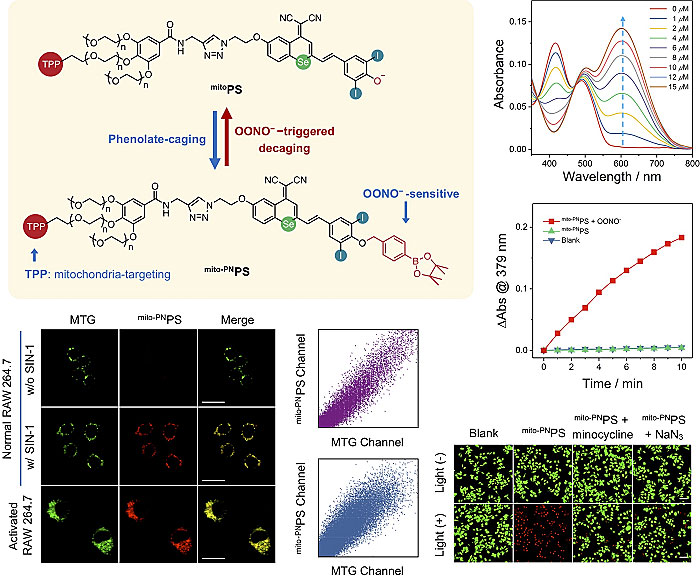
通过酯化或醚化反应,将PSSe-I骨架中作为电子给体的酚羟基笼蔽之后,其ICT过程被成功阻断并伴随可见光区的吸收峰完全消失,导致光敏性能被彻底抑制。在特定刺激物(如碱性磷酸酶或活性氧簇)作用下,酚羟基的保护基被迅速切除并释放电子给体,恢复高效光敏性能,实现了应激开启。为了促进更多的功能集成,研究人员在PSSe-I的骨架上引入叠氮基团,并通过点击化学反应成功制备了线粒体靶向的激活型光敏剂。
该激活机制实现了激活型光敏剂从彻底抑制到应激开启的光敏性能转变,同时得益于酚羟基保护化学及点击化学的灵活性,这项工作为按需定制激活型光敏剂提供了一个通用平台,以更好的服务于肿瘤的特异性光动力治疗。
相关结果发表Angewandte Chemie International Edition 上,文章的第一作者是南开大学的博士研究生翟文豪。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

De Novo Designed Highly Efficient Photosensitizer as a Universal Scaffold for Activatable Photosensitizer with Completely Inhibited Photosensitivity
Wenhao Zhai, Yongkang Zhang, Ming Liu, Hao Zhang, Junqing Zhang, Changhua Li
Angew. Chem. Int. Ed., 2019, DOI: 10.1002/anie.201907510
导师介绍
李昌华
https://www.x-mol.com/university/faculty/73328
(本稿件来自Wiley)
 0
0












