芬顿反应最早由法国化学家Fenton在1893年发现,并因其能产生强氧化性的羟基自由基等活性氧物种(ROS)被广泛应用于水中有机污染物的去除。理想的芬顿反应是Fe2+催化H2O2生成羟基自由基等ROS,但实际上,大多数已报道的芬顿反应并不是真正的催化反应,而只是一个氧化还原化学反应。这主要是因为当Fe2+活化H2O2(或PMS)后,本身会被氧化成Fe3+,而Fe3+很难被H2O2重新还原成Fe2+,所以铁在芬顿反应中不能算真正的催化剂。好消息是,通过引入助催化剂可以很好地解决这个问题。比如,邢明阳等人首次发现通过引入MoS2作为助催化剂,可以实现芬顿反应中铁离子的高效循环(Chem, 2018, 4, 1359-1372)。但这也带来了新的问题,即大多数粉体催化剂的共同缺点就是难以在实际应用中回收再利用,尤其是在大规模处理实际工业废水时,需要不断的补充MoS2助催化剂及铁催化剂,这不仅会增加反应成本,还会存在对环境造成二次污染的风险。
图1. 三维MoS2海绵助催化(类)芬顿体系的构建及其用于水污染控制
为了克服上述挑战,华东理工大学邢明阳教授(点击查看介绍)研究团队采用简单的浸渍-加热的化学方法,开发了三维硫化钼(3D-MoS2海绵)助催化(类)芬顿反应体系,实现了对染料类及抗生素类废水的高效处理。与传统芬顿体系及已报道的助催化(类)芬顿体系相比,其优势表现为:1)三维结构优化AOPs性能优势。以Fe3+/H2O2体系为例,3D-MoS2海绵的引入,可使其降解芳香族有机污染物的反应速率常数提高到原来的52倍;2)助催化反应中心减少铁的用量,降低生成铁泥的风险。3D-MoS2海绵中纳米花片层堆积和不规则边缘可以提供更多的Mo4+活性位点,加速Fe3+/Fe2+的循环,抑制铁泥等二次污染物的形成;3)运行成本低,实现大规模高效处理抗生素废水。3D-MoS2/Fe2+/PMS体系只需一次性加入铁离子(20 mg/L硫酸亚铁),即可实现连续高效处理140 L高浓度磺胺嘧啶废水(120 mg/L),其降解率可达97.87%,该体系可稳定运行16天以上。且其处理1吨废水的运行成本仅为0.33美元,使其具有巨大的工业应用价值。
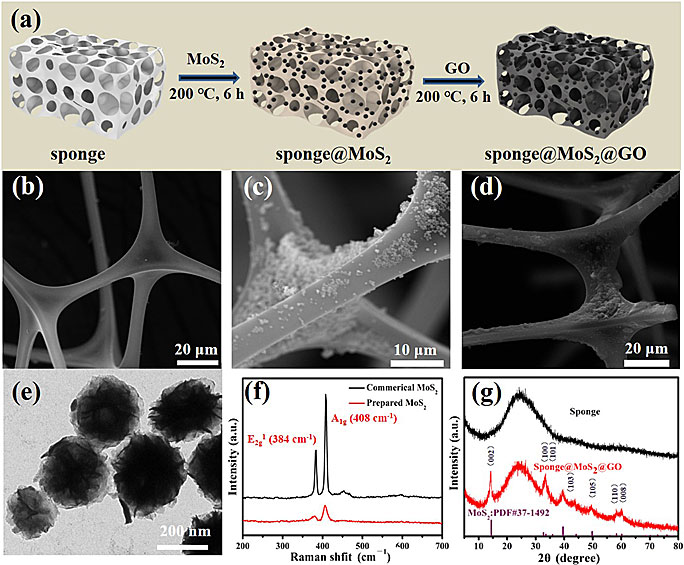
图2. (a) 3D-MoS2海绵合成途径示意图; (b)空白海绵,(c) 3D-MoS2海绵(不含GO),(d) 3D-MoS2海绵(含GO)的SEM照片; (e) 化学法制备的MoS2纳米球的TEM照片; (f) MoS2纳米球的拉曼光谱; (g) 3D-MoS2海绵的XRD图谱
采用简单的浸渍-加热相结合的方法将GO与MoS2纳米球负载在海绵的内外表面,成功制备了3D-MoS2海绵(如图2a所示)。SEM电镜照片显示,MoS2纳米球被均匀负载在海绵的骨架上(MoS2负载量只有0.94wt%,节约了催化剂成本),GO的引入可以有效防止MoS2的脱落(图2b-d)。GO的引入不仅可以增加MoS2海绵的机械强度,还使其表面具有一定的疏水性(漂浮在水面),更有利于催化剂的回收。MoS2纳米球的层状堆积和不规则边缘可以提高其比表面积和吸附性能,其花瓣状的边缘提供了更多的不饱和硫活性位点(图2e)。与商品化硫化钼相比,3D-MoS2的结晶度相对较弱,说明其表面存在大量硫缺陷(Mo4+活性位点,图2f-g),更有利于助催化反应的发生。
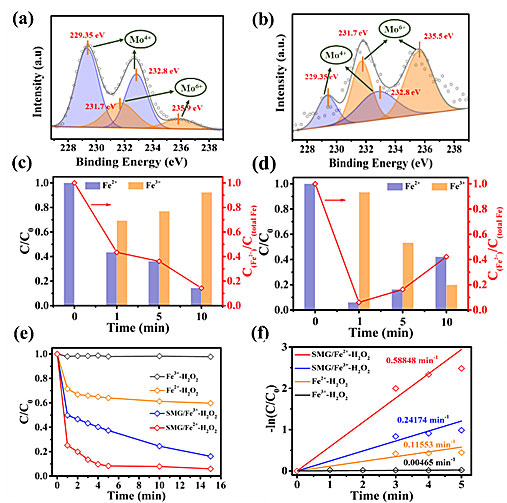
图3. 3D-MoS2海绵在反应(a)前(b)后的Mo 3d XPS图谱; (c)传统Fenton体系和(d) 1SMG/Fe2+-H2O2体系中Fe3+和Fe2+的浓度变化; (e) 分别以Fe3+和Fe2+为催化剂降解RhB的缺陷图,及(f)相应的RhB降解速率常数(实验中使用的Fe3+为硫酸铁)。
为了探索1SMG在1SMG/Fe2+-H2O2体系中的协同催化机制,首先用XPS研究了1SMG表面化学环境的变化。从图3a-b可以看出,SMG表面的不饱和S原子使其表面暴露大量Mo4+还原活性位点。反应后,Mo4+峰强度减弱,Mo6+峰强度增强,说明Fenton反应中部分暴露的Mo4+被表面吸附的Fe3+氧化为Mo6+。在反应过程中,传统Fenton体系中Fe2+浓度不断降低(图3c),Fe3+浓度不断升高,说明Fe2+不断被消耗形成Fe3+,最终形成铁泥等二次污染物(Fe(OH)x等)。而在1SMG/Fe2+-H2O2体系中(图3d),随着反应的进行,Fe2+先快速下降,然后逐渐升高。说明添加1SMG可以提高Fe3+向Fe2+的转换效率,从而抑制铁泥的形成,促进H2O2分解生成•OH。通过HPLC-MS研究了有机分子的消除机制,发现•OH作为主要活性物种,具有良好的氧化性能,能将芳香族有机污染物分解为小分子脂肪酸和短链烯烃。首先,这些有机物被•OH破坏,例如,破坏双键,攻击孤电子对,打开苯环,形成单环或线性结构的小分子。然后•OH继续在小分子上进行自由基反应,直到最终把其矿化为 CO2和水。值得注意的是,与Fe2+相比,Fe3+更便宜且更容易获得,但其催化H2O2的效率太低。以Fe3+为催化剂,通过引入3D-MoS2海绵作为助催化剂,可以使其芬顿反应降解RhB的活性提高52倍(反应速率常数从0.00465提高到0.24174 cm-1 (图3e-f))。Fe3+作为铁最稳定的离子态,广泛存在于废钢渣和铁渣中。在这里,作者证明了加入3D-MoS2海绵可以实现Fe3+到Fe2+的高效转化。这意味着未来Fenton反应可以利用废钢渣或铁渣作为铁源,不仅变废为宝,还可进一步降低Fenton反应处理有机污染物废水的成本。
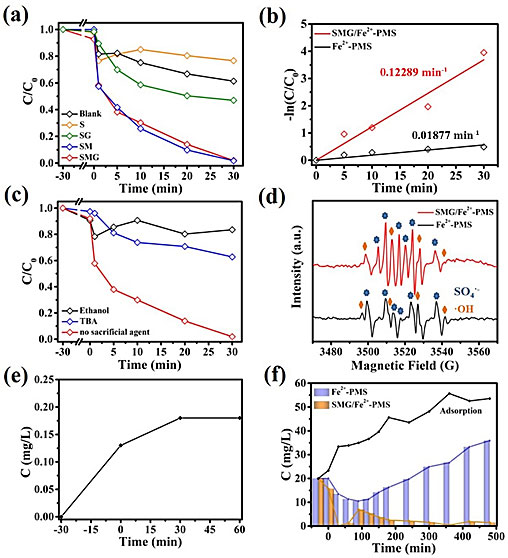
图4. (a)不同助催化剂(海绵、1SM、SG、1SMG)在Fe2+-PMS体系中对磺胺嘧啶(SD)的降解; (b) SD在传统Fe2+-PMS和1SMG/Fe2+-PMS体系中的降解速率常数; (c) 在1SMG/Fe2+-PMS体系中加入乙醇或t-丁醇(TBA)的牺牲实验; (d) EPR谱检测•OH和SO4·- ; (e) 钼离子的溶出实验; (f) 当系统扩大到400 mL时,高浓度SD的持续降解,将传统的Fe2+-PMS体系与1SMG/Fe2+-PMS体系进行比较,黑线为对比的吸附实验(降解反应持续8个小时,加药12次,每次加4 ml (15 mg/ml)的PMS和2 ml (2 mg/ml)的SD)。
加入1SMG作为助催化剂,PMS体系对于SD的去除率从38.6%升高到98.3%(图4a),对应的降解速率常数提高到原来的6.5倍(图4b),表明3D-MoS2海绵同样可以高效助催化类芬顿反应分解PMS。牺牲剂实验与EPR数据表明(图4c,d),1SMG/Fe2+-PMS体系中生成的•OH与SO4·-的量比为2:1,且•OH与SO4·-对有机物的降解起着重要作用。图4e为1SMG/Fe2+-PMS体系中钼离子的溶出实验。可以看出,负载在1SMG表面的MoS2在吸附30 min和降解30 min时均有少量溶解,在降解30 min内保持平衡。这两个过程中Mon+的总溶出浓度仅为0.18 mg/L,且不会持续溶出,说明1SMG在整个反应过程中非常稳定,MoS2在海绵表面也足够稳定,对环境没有造成显著的二次污染。作者用400 ml体系进行了8小时的连续降解SD实验(图4f)。传统Fe2+-PMS体系中SD的浓度不断升高,最终达到35.8 mg/L。但1SMG/Fe2+-PMS体系中SD浓度在8 h后维持在1.5 mg/L,说明负载的MoS2可以稳定系统中的Fe2+,并持续促进PMS分解生成活性物质,从而维持持续降解。为了排除1SMG的吸附效果,在相同条件下进行吸附实验,不添加PMS。随着高浓度溶液的加入,SD浓度不断增加,最终接近53.5 mg/L。这说明,SD的良好去除率并不是由于1SMG的吸附造成的。值得一提的是,整个连续反应过程只加入了一次铁离子(20 mg/L硫酸亚铁),且没有观察到铁泥的生成。这一结果对于解决工业应用中铁泥的生成具有十分重要的意义。
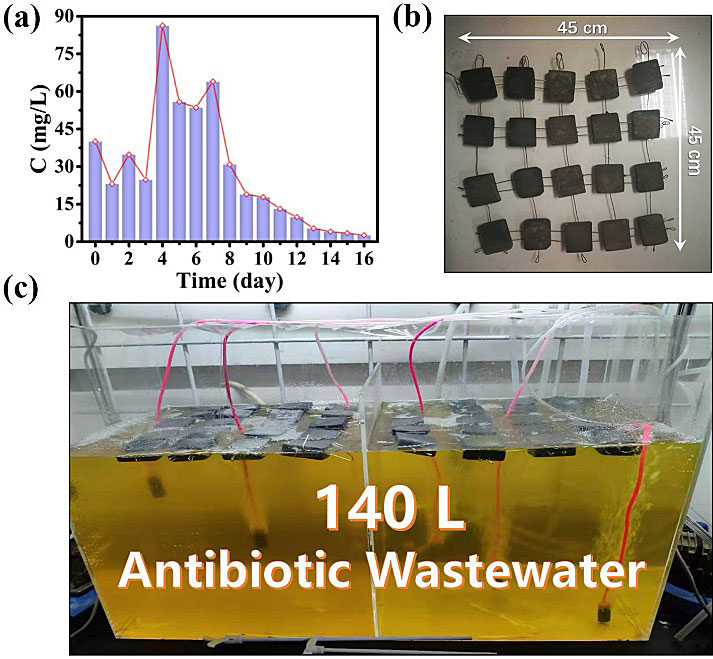
图5. 中试试验: (a) 140 L SD连续降解16天(SD总浓度:120 mg/L); (b) 放大生产3D-MoS2海绵的产品照片; (c) 140 L 中试反应器照片。
这通过以上反应条件的摸索及反应机理的研究,作者对1SMG/Fe2+-PMS体系进行了降解SD的中试规模实验(图5)。3D-MoS2海绵模块可以稳定漂浮在水面上,确保降解后可以很容易回收再利用。这不仅节约了成本,还不会对环境造成二次污染。将140 L含SD污染物的自来水加入90 cm* 40 cm* 60 cm透明有机玻璃缸中。放入3D-MoS2海绵模块,每隔2小时空气鼓泡2小时。只在反应初始时一次加入2.8 g的硫酸亚铁(后续不再补充铁),每天加入10 g的PMS,每隔一天加入5.6 g的SD,一直加到SD的总浓度达到120 mg/L,连续反应16天。结果发现(图5a),1SMG/Fe2+-PMS体系可实现对大规模抗生素废水长期稳定的降解,SD浓度一直维持在一个比较低的水平,反应16天后,SD的浓度降至2.56 mg/L去除率高达97.87%。根据中试试验结果,以1吨20 mg/L的SD废水为例,对运行成本进行评估:1SMG/Fe2+-PMS体系不需要任何特殊的反应器条件,只需要常规曝气处理,体系运行成本仅为0.33美元/吨,远低于大部分已报道的其它类芬顿反应体系,具有巨大的工业应用前景。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Designing 3D-MoS2 Sponge as Excellent Cocatalysts in Advanced Oxidation Processes for Pollutant Control
Lingli Zhu, Jiahui Ji, Jun Liu, Shinya Mine, Masaya Matsuoka, Jinlong Zhang, Mingyang Xing*
Angew. Chem. Int. Ed., 2020, DOI: 10.1002/anie.202006059
导师介绍
邢明阳
https://www.x-mol.com/groups/xing_mingyang
 0
0











