当纳米材料进入生物环境中(例如血液),由于其大的比表面积和高的吸附活性,表面会吸附大量的血浆蛋白,形成蛋白冠(protein corona)。这层蛋白质冠的形成不仅会影响蛋白质分子本身的结构和生物功能,同时也会改变纳米材料的生物学行为。因此,如何理解纳米材料与血浆蛋白的作用,特别是精确调控纳米材料表面蛋白冠的组成,对在生物医学领域更好地利用纳米材料乃至未来个性化的医学治疗至关重要。
最近,南京大学马余强教授课题组与苏州大学丁泓铭副教授、南京医科大学霍达教授等合作,通过结合理论模拟与实验,提出了一种可以有效操控纳米材料表面蛋白冠成分的简单方法,并从分子、细胞和组织层次揭示了纳米材料表面修饰对其在生物体内代谢影响的内在机理。
在这项工作中,作者首先通过全原子分子动力学模拟研究了三种典型血浆蛋白(HAS、IgE、ApoE)与不同表面修饰的石墨烯作用机理。研究发现,随着石墨烯表面羟基数目的增多,HSA与IgE的吸附面积逐渐下降(图1a-b);而ApoE的吸附面积却与石墨烯表面羟基数目无明显关联(图1c)。通过进一步分析蛋白质吸附到石墨烯上的构象,他们发现二级结构的变化是影响蛋白质吸附面积的关键因素——对于具有疏水内核结构的HSA和以beta片为主的IgE而言,随着纳米材料亲水度的增加,二级结构破坏逐渐减弱,从而吸附面积逐渐降低;而对于以alpha结构为主和亲疏水相间的ApoE而言,亲水和疏水表面对其二级结构的破坏无明显差别,从而其吸附面积没有太大区别(图1d)。以上结果也得到了蛋白质体外吸附实验的证实(图1e),即通过调控纳米材料表面亲疏水性可以有效地调控纳米材料的蛋白冠成分。此外,他们还以金纳米材料为例,进一步地证明了这一结果的普适性(图2)。
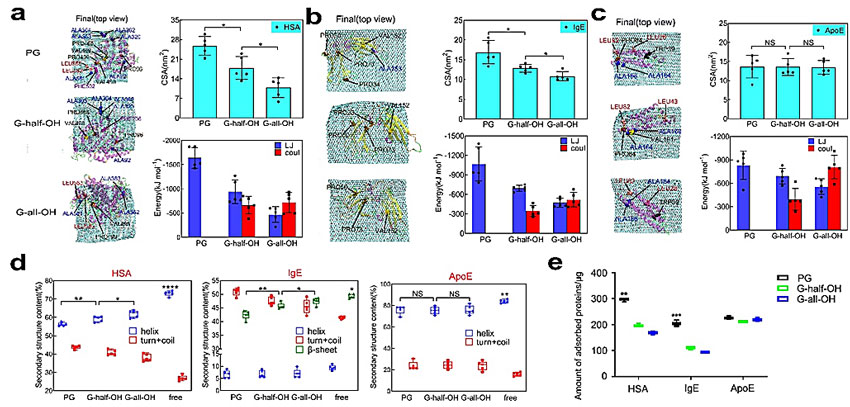
图1. 不同表面修饰石墨烯与三种血浆蛋白相互作用的全原子模拟和体外实验结果。
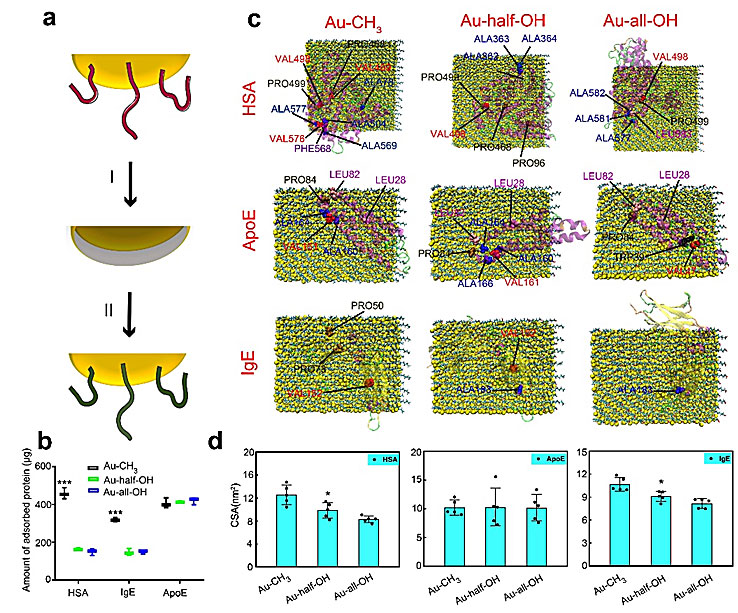
图2. 不同表面修饰金纳米粒子与三种血浆蛋白相互作用的全原子模拟和体外实验结果。
通常HSA和IgE(特别是IgE)的吸附会提高纳米材料被免疫系统清除的概率,而ApoE的吸附则会降低纳米材料被免疫系统识别的可能性。目前工作的重要性还在于他们通过简单地调控纳米材料表面的亲疏水度,可以显著地降低HSA和IgE在纳米材料表面的吸附行为,而同时对ApoE的吸附不会造成太大影响(特别当羟基在纳米材料表面呈现两面神型分布时,ApoE的吸附面积会进一步提高),从而能够极大地提高纳米材料在血液中的循环时间和达到肿瘤组织的数量。相关的体内实验完全验证了这一想法(图3);此外作者还发现通过预吸附ApoE在纳米材料表面,能够进一步提高纳米材料在肿瘤组织的富集量。
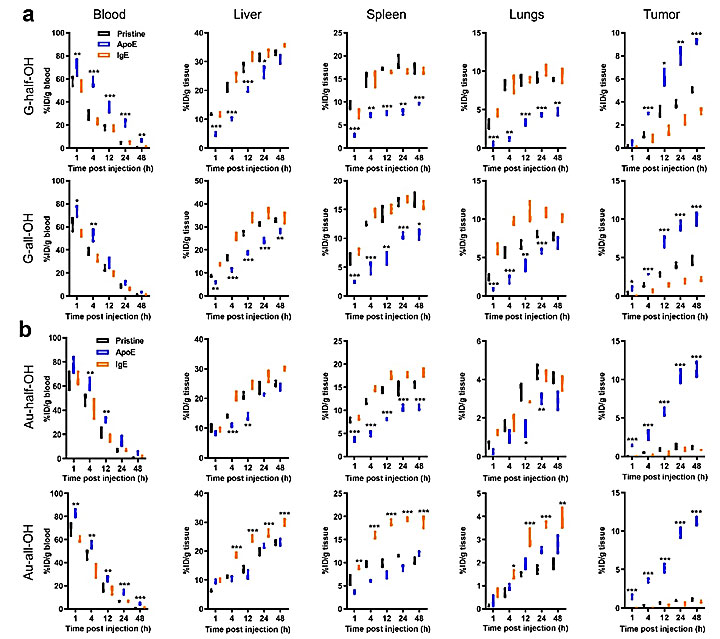
图3. 不同表面修饰纳米材料的体内分布和代谢行为。
相关成果发表Nature Communications 上,南京大学博士研究生卢翔和鼓楼医院许佩佩博士是论文的并列第一作者,南京大学马余强教授、苏州大学丁泓铭副教授和南京医科大学霍达教授是论文的共同通讯作者。该工作得到固体微结构物理国家重点实验室和人工微结构科学与技术协同创新中心,以及国家自然科学基金等项目的资助。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Tailoring the component of protein corona via simple chemistry
Xiang Lu, Peipei Xu, Hong-Ming Ding, You-Sheng Yu, Da Huo, Yu-Qiang Ma
Nat. Commun., 2019, 10, 4520, DOI: 10.1038/s41467-019-12470-5
研究团队简介
马余强,南京大学物理学院教授。主要从事物理学与化学和生命科学交叉的软凝聚态物理研究,发表国际学术刊物论文两百余篇,包括作为通信联系人身份发表在国际权威综合性刊物如Nature Nanotechnology、Nature Communications、PNAS以及多次受邀撰写综述性评述发表在Chem Soc Rev、Nanoscale Horizons、Small、Soft Matter 等。发表的论文中有10余篇为封面论文或热点论文。 曾于1999年荣获国家杰出青年科学基金、2001年入选教育部长江学者奖励计划。培养学生中有10余位为高等学校教授。
https://www.x-mol.com/university/faculty/45873

丁泓铭,苏州大学物理科学与技术学院副教授。2010年、2015年分别于南京大学物理学院取得学士、博士学位(导师:马余强教授),2015年8月起就职于苏州大学软凝聚态物理及交叉研究中心。主要从事计算软物质物理、纳米-生物界面相互作用及自组装等方面的理论模拟研究。在相关领域发表SCI论文近40篇。以第一作者(含并列一作)和通讯作者身份在Nature Communications(2篇), Journal of American Chemical Society(3篇), ACS Central Science, Angewandte Chemie International Edition, ACS Nano(2篇), Biomaterials(3篇), Small 等SCI杂志发表论文30余篇,包括8篇封面论文,3篇曾入选ESI高被引论文。目前主持国家自然科学基金面上项目、青年基金各一项,入选苏州大学首批优秀青年学者及苏州市高等院校、科研院所紧缺高层次人才。

霍达,1987年9月生于吉林长春,教授,博士生导师。2010和2015年于南京大学现代工程与应用科学学院分别获得理学学士学位和工学博士学位(导师:胡勇教授),博士后研究结束后于2019年6月加盟南京医科大学药学院。主要研究兴趣包括纳米药物载体的表面效应与药代动力学,毒理学,及表观遗传学之间的关联。近五年围绕亚细胞精准定位的纳米药物载体设计及其蛋白冠效应分析,疾病微环境相应性诊疗一体化纳米系统的开发,和纳米材料界面-细胞作用机制等方向取得了一系列原创性的研究成果,以通讯作者,第一作者(含并列一作)身份发表论文23篇,包括Nature Communications (2篇),Journal of American Chemical Society, Advanced Materials, ACS Nano, Advanced Functional Materials, Nano Letters, Chemical Reviews各1篇,Biomaterials (6篇)。
 0
0










